
【题目】室温下,下列溶液中粒子浓度关系正确的是( )
A.0.01mol·L-1H2S溶液:c(H+)>c(HS-)>c(S2-)>c(H2S)>c(OH-)
B.![]() =10-10的Na2CO3溶液:c(HCO3-)+2c(H2CO3)=c(10-2-10-12)mol·L-1
=10-10的Na2CO3溶液:c(HCO3-)+2c(H2CO3)=c(10-2-10-12)mol·L-1
C.等物质的量的NH4Cl和NaCl的混合溶液:c(NH4)+c(NH3·H2O)+c(Na+)=2c(Cl-)
D.0.1mol·L-1NaHSO3溶液:c(Na+)+c(H+)<c(HSO3-)+c(SO32-)+c(OH-)
【答案】B
【解析】
A. 0.01mol·L-1H2S溶液呈酸性,H2S分两步电离分别生成HS-和S2-,第一次电离比第二次电离程度大,溶液中各物质浓度大小关系为:c(H2S)> c(H+)>c(HS-)>c(S2-)>c(OH-),故A错误;
B. 室温下,Na2CO3溶液中存在c(H+) c(OH-)=10-14,结合![]() =10-10可得c(H+)=10-12,c(OH-)=10-2,电荷守恒:c(Na+) + c(H+) = c(OH-) +2c(CO32-)+ c(HCO3-);物料守恒:c(Na+)= 2 c(H2CO3)+2c(HCO3-) +2c(CO32-);根据电荷守恒式和物料守恒式得出质子守恒式:2 c(H2CO3)+ c(HCO3-) + c(H+)= c(OH-);则c(HCO3-)+2c(H2CO3)= c(OH-)- c(H+)= c(10-2-10-12)mol·L-1,故B正确;
=10-10可得c(H+)=10-12,c(OH-)=10-2,电荷守恒:c(Na+) + c(H+) = c(OH-) +2c(CO32-)+ c(HCO3-);物料守恒:c(Na+)= 2 c(H2CO3)+2c(HCO3-) +2c(CO32-);根据电荷守恒式和物料守恒式得出质子守恒式:2 c(H2CO3)+ c(HCO3-) + c(H+)= c(OH-);则c(HCO3-)+2c(H2CO3)= c(OH-)- c(H+)= c(10-2-10-12)mol·L-1,故B正确;
C. 因为NH4Cl和NaCl等体积混合,所以氮原子:氯原子=1:2,c(Na+)= c(Cl-)所以氯离子浓度就等于所有含氮物质浓度之和的两倍,也就是2c(NH4)+ 2c(NH3·H2O)=c(Cl-),则c(NH4)+c(NH3·H2O)+c(Na+)= ![]() c(Cl-),故C错误;
c(Cl-),故C错误;
D. 0.1mol·L-1NaHSO3溶液中有电荷守恒:c(Na+)+c(H+)=c(HSO3-)+2c(SO32-)+c(OH-),则c(Na+)+c(H+)>c(HSO3-)+c(SO32-)+c(OH-),故D错误;
正确答案是B。


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
【题目】有X、Y、Z、W四种含14个电子的粒子,其结构特点如下:
粒子代码 | X | Y | Z | W |
原子核数 | 单核 | 不同元素构成的两核 | 同元素构成的两核 | 同元素构成的两核 |
粒子的电荷数 | 0 | 0 | 两个负电荷 | 0 |
![]() 原子核外比X原子多3个电子,A的原子结构示意图是 ______ 含
原子核外比X原子多3个电子,A的原子结构示意图是 ______ 含![]() 的氧化物晶体中含有共价键数目为 ______
的氧化物晶体中含有共价键数目为 ______
![]() 与钙离子组成的化合物的电子式为 ______
与钙离子组成的化合物的电子式为 ______
![]() 完全燃烧放出的热量是
完全燃烧放出的热量是![]() ,写出Y燃烧的热化学方程式 ______
,写出Y燃烧的热化学方程式 ______
![]() 组成W的元素最高价氧化物对应的水化物甲有如图所示转化关系
组成W的元素最高价氧化物对应的水化物甲有如图所示转化关系![]() 反应条件和其他物质已略
反应条件和其他物质已略![]()
![]()
![]() 写出丁在高温下与水反应的化学方程式 ______
写出丁在高温下与水反应的化学方程式 ______
![]() 组成W的元素的简单氢化物极易溶于水的主要原因是 ______ ,该氢化物与空气可以构成一种燃料电池,电解质溶液是KOH,其负极的电极反应式为 ______ 。
组成W的元素的简单氢化物极易溶于水的主要原因是 ______ ,该氢化物与空气可以构成一种燃料电池,电解质溶液是KOH,其负极的电极反应式为 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“变化观念与平衡思想”是化学学科的核心素养,室温时,0.1 mol·L1草酸钠溶液中存在多个平衡,其中有关说法正确的是[己知室温时,Ksp(CaC2O4)=2.4×109]
A. 若将溶液不断加水稀释,则水的电离程度增大
B. 溶液中各离子浓度大小关系:c(Na+)> c(C2O42)> c(OH)> c(H+)> c(HC2O4)
C. 若用pH计测得溶液的pH=9,则H2C2O4的第二级电离平衡常数Ka2=105
D. 向溶液中加入等体积CaCl2溶液,当加入的CaCl2溶液浓度大于2.4×108 mol·L1 时即能产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取10g碳酸钙高温加热一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%,则下列判断正确的是
A.生成了2g二氧化碳B.剩余固体质量为5g
C.生成了5.6g氧化钙D.剩余碳酸钙的质量为8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,两种不同浓度的NaOH溶液中,c(H+)分别为1×10-14 mol·L-1和1×10-10 mol·L-1。将这两种溶液等体积混合后,所得溶液中c(H+)是
A. 1×(10-14+10-10) mol·L-1 B. ![]()
![]() mol·L-1
mol·L-1
C. 2×10-10 mol·L-1 D. 2×10-14 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂空气电池是一种新型的二次电池,其放电时的工作原理如图所示。下列说法正确的是( )
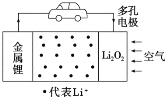
A.电解液中,Li+由多孔电极迁移向锂电极
B.该电池放电时,负极发生了还原反应
C.充电时,电池正极的反应式为Li2O2-2e-=2Li++O2↑
D.电池中的电解液可以是有机电解液或稀盐酸等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案不能达到实验目的的是

A. 图A装置Cu和浓硝酸制取NO B. 图B装置实验室制备Cl2
C. 图C装置实验室制取乙酸乙酯 D. 图D装置实验室分离CO和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

(1)氢氧燃料电池的能量转化主要形式是___,在导线中电子流动方向为___(用a、b和箭头表示)。
(2)正极反应的电极反应方程式为___。
(3)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

①图1中N型半导体为___(填“正极”或“负极”)
②该系统工作时,A极的电极反应式为___。
③若A极产生7.00gN2,则此时B极产生___LH2(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10mL浓度为0.1mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A.水的电离程度始终增大
B.![]() 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com