
常温下,下列离子浓度的关系正确的是 ( )
A.pH=2的盐酸与pH=12的氨水等体积混合:
c(NH )=c(Cl-)>c(H+)=c(OH-)
)=c(Cl-)>c(H+)=c(OH-)
B.0.2 mol·L-1的CH3COONa溶液与0.1 mol·L-1的HCl等体积混合:
c(Na+)>c(Cl-)>c(CH3COO-)>c(H+)>c(OH-)
C.0.1 mol·L-1的HCN(弱酸)和0.1 mol·L-1的NaCN等体积混合:
c(HCN)+c(CN-)+c(OH-)=c(Na+)+c(H+)
D.相同物质的量浓度时,溶液中c(NH )由大到小的顺序:NH4Al(SO4)2>NH4Cl>CH3COONH4>NH3·H2O
)由大到小的顺序:NH4Al(SO4)2>NH4Cl>CH3COONH4>NH3·H2O
科目:高中化学 来源: 题型:
研究钠及其化合物有重要意义。
(1)NaOH是实验室中最常用的试剂之一。实验室进行某实验需要0.5 mol·L-1的氢氧化钠溶液约480 mL,根据溶液配制的过程,回答下列问题:
①实验除了需要托盘天平(带砝码)、药匙、烧杯和玻璃棒外,还需要的其他玻璃仪器
是 。
②根据计算得知,需用托盘天平(带砝码)准确称量NaOH固体 g。
⑵Na2O2可作为呼吸面具和潜水艇里氧气的来源。Na2O2作为供氧剂时可能发生的反应
有 、 。
⑶NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。
已知NaNO2能发生如下反应: 2NaNO2+4HI===2NO↑+I2+2NaI+2H2O
①上述反应中,氧化剂是________。每生成标准状况下的NO气体2.24L,反应中被氧化的HI 的物质的量是 mol。
②某厂废切削液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是________。
A.NaCl B.NH4Cl C.HNO3 D.浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生产、生活、社会密切相关。下列有关说法中,正确的是
A.明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒
B.SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆
C.鼓励汽车、家电“以旧换新”,可减少环境污染,发展循环经济,促进节能减排
D.焰火“脚印”、“笑脸”,使北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”的知识相关,焰色反应是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
2SO2(g)+O2(g)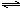 2SO3(g) △H=-196.4kJ·mol-1
2SO3(g) △H=-196.4kJ·mol-1
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中 的能量变化 | ||
| SO2 | O2 | SO3 | ||
| ① | 2 | 1 | 0 | 放出热量a kJ |
| ② | 1 | 0.5 | 0 | 放出热量b kJ |
| ③ | 0 | 0 | 2 | 吸收热量c kJ |
下列叙述不正确的是
A.平衡时SO3气体的体积分数:③=①>② B.a+c=196.4
C.三个容器内反应的平衡常数:③=①=② D.平衡时O2的浓度:①=③=2×②
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.在一定温度下的AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数
B.AgCl的Ksp=1.8×10-10 mol2·L-2,在任何含AgCl固体的溶液中,[Ag+]=[Cl-],且Ag+和Cl-浓度的乘积等于1.8×10-10mol2·L-2
C.温度一定时,在AgCl饱和溶液中,Ag+和Cl-浓度的乘积是一个常数
D.向饱和AgCl溶液中加入盐酸,Ksp变大
查看答案和解析>>
科目:高中化学 来源: 题型:
有①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25 mL,物质的量浓度均为0.1 mol·L-1,下列说法正确的是 ( )
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25 mL 0.1 mol·L-1的盐酸后,pH最大的是①
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃时部分弱电解质的电离平衡常数数据如下表:
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.7×10-5 | 6.2×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
回答下列问题:
(1)写出碳酸的第一级电离平衡常数表达式:K1=_______________________。
(2)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为 ___ _____(填字母)。
(3) 常温下,0.1 mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 (填序号)
A.[H+] B.[H+]/[CH3COOH] C.[H+]·[OH-] D.[OH-]/[H+]
 (4)25 ℃时,将20 mL 0.1 mol·L-1 CH3COOH溶液和20mL0.1 mol·L-1HSCN溶液分别与20 mL 0.1 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如右图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是
(4)25 ℃时,将20 mL 0.1 mol·L-1 CH3COOH溶液和20mL0.1 mol·L-1HSCN溶液分别与20 mL 0.1 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如右图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是
反应结束后所得两溶液中,c(CH3COO-)________c(SCN-)(填“>”、“<”或“=”)
 (5)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(5)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(6)25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=________mol·L-1(填精确值),
c(CH3COO-)/c(CH3COOH)=________。
(7) 写出少量CO2通入次氯酸钠溶液中的离子方程式:
______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
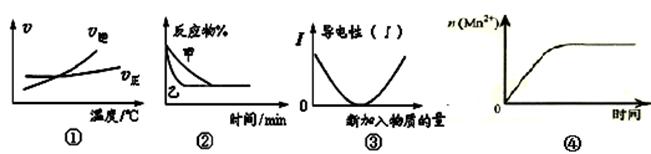
下列图像描述正确的是
A.由图①可判断可逆反应A2(g)+3B2(g) 2AB3(g)正反应是放热反应
2AB3(g)正反应是放热反应
B.图②表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D.图④表示10 mL 0.01 mol·L-1 KMnO4酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各溶液中,Na+浓度最大的是( )
A.4 L 0.5 mol·L-1的NaCl溶液 B.1 L 0.3 mol·L-1的Na2SO4溶液
C.0.8 L 0.4 mol·L-1的NaOH溶液 D.2 L 0.15 mol·L-1的Na3PO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com