
 .
. .
. .
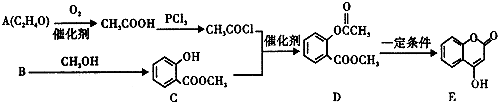
. 分析 (1)B与甲醇发生酯化反应得到C,可推知B为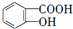 ,A发生氧化反应生成乙酸,则A为CH3CHO;
,A发生氧化反应生成乙酸,则A为CH3CHO;
(2)对比C、D结构可知,C中酚羟基中H原子被-COCH3取代生成D;E中苯环与C=C双键与氢气发生加成反应;
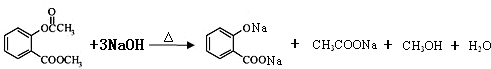
(3)D中存在酯基,在碱液中可以发生水解反应,水解生成的羧基、酚羟基与NaOH发生中和反应,反应生成 、CH3COONa、CH3OH;
、CH3COONa、CH3OH;
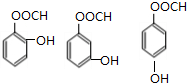
(4)B为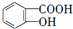 ,B的同分异构体符合:能够发生银镜反应,说明含有醛基;能与FeCl3溶液发生显色反应,含酚羟基,1mol该同分异构体与NaOH溶液反应时,最多可消耗3mol NaOH,则含有甲酸与酚形成的酯基,有邻、间、对3种;
,B的同分异构体符合:能够发生银镜反应,说明含有醛基;能与FeCl3溶液发生显色反应,含酚羟基,1mol该同分异构体与NaOH溶液反应时,最多可消耗3mol NaOH,则含有甲酸与酚形成的酯基,有邻、间、对3种;
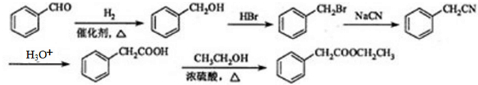
(5)苯甲醛与氢气发生加成反应生成苯甲醇,再发生取代反应生成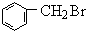 ,与NaCN发生取代反应得到
,与NaCN发生取代反应得到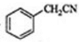 ,再水解得到苯乙酸,苯乙酸与乙醇发生酯化反应得到苯乙酸乙酯.
,再水解得到苯乙酸,苯乙酸与乙醇发生酯化反应得到苯乙酸乙酯.
解答 解:(1)B与甲醇发生酯化反应得到C,可推知B为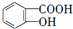 ,含有官能团为羧基、羟基,A发生氧化反应生成乙酸,则A为CH3CHO,含有官能团为醛基,用银氨溶液或新制氢氧化铜悬浊液检验醛基,
,含有官能团为羧基、羟基,A发生氧化反应生成乙酸,则A为CH3CHO,含有官能团为醛基,用银氨溶液或新制氢氧化铜悬浊液检验醛基,
故答案为:羧基、羟基;银氨溶液或新制氢氧化铜悬浊液;
(2)对比C、D结构可知,C中酚羟基中H原子被-COCH3取代生成D,属于取代反应;E中苯环与C=C双键与氢气发生加成反应,故1mol E最多可与4mol H2反应,
故答案为:取代反应;4;
(3)D中存在酯基,在碱液中可以发生水解反应,水解生成的羧基、酚羟基与NaOH发生中和反应,反应生成 、CH3COONa、CH3OH,反应方程式为:
、CH3COONa、CH3OH,反应方程式为: ,
,
故答案为: ;
;
(4)B为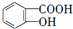 ,B的同分异构体符合:能够发生银镜反应,说明含有醛基;能与FeCl3溶液发生显色反应,含酚羟基,1mol该同分异构体与NaOH溶液反应时,最多可消耗3mol NaOH,则含有甲酸与酚形成的酯基,有邻、间、对3种,符合条件的同分异构体结构简式为:
,B的同分异构体符合:能够发生银镜反应,说明含有醛基;能与FeCl3溶液发生显色反应,含酚羟基,1mol该同分异构体与NaOH溶液反应时,最多可消耗3mol NaOH,则含有甲酸与酚形成的酯基,有邻、间、对3种,符合条件的同分异构体结构简式为: ,
,
故答案为: ;
;
(5)苯甲醛与氢气发生加成反应生成苯甲醇,再发生取代反应生成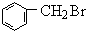 ,与NaCN发生取代反应得到
,与NaCN发生取代反应得到 ,再水解得到苯乙酸,苯乙酸与乙醇发生酯化反应得到苯乙酸乙酯,合成路线流程图为:
,再水解得到苯乙酸,苯乙酸与乙醇发生酯化反应得到苯乙酸乙酯,合成路线流程图为: ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成,充分利用有机物的结构进行分析解答,熟练掌握官能团的性质与转化,侧重考查学生分析推理能力.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:选择题
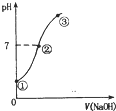 常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )| A. | ①点所示溶液中只存在HC1O的电离平衡 | |
| B. | ②到③的过程中水的电离程度一定减少 | |
| C. | ②点处表示氯气与氢氧化钠溶液恰好反应完全 | |
| D. | ②点所示溶液中:c( Na+)=c(C1-)+c(ClO -) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 牙膏品牌 | 两面针儿童牙膏 | 中华透明牙膏 | 珍珠防臭牙膏 |
| 摩擦剂 | 氢氧化铝 | 二氧化硅 | 碳酸钙 |
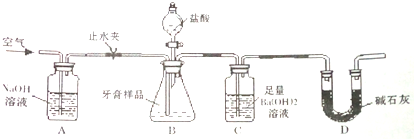
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜粉加入到Fe2(SO4)3溶液中:Cu+Fe3+═Cu2++Fe | |
| B. | 钠块投入到CuSO4溶液中:2Na+Cu2+═2Na++Cu↓ | |
| C. | Cl2通入到NaOH溶液中:Cl2+2OH-═Cl-+ClO-+H2O | |
| D. | 用NaOH溶液吸收少量CO2:OH-+CO2═HCO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
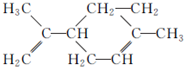 ,有关柠檬烯的说法正确的是( )
,有关柠檬烯的说法正确的是( )| A. | 柠檬烯分子为非极性分子 | |
| B. | 柠檬烯分子中所有碳原子处于同一个平面上 | |
| C. | 柠檬烯能与酸性高锰酸钾溶液发生取代反应 | |
| D. | 柠檬烯的分子式为C10H16,能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),曲线a表示该反应在温度T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.叙述正确的是( )
一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),曲线a表示该反应在温度T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.叙述正确的是( )| A. | 温度T℃时,该反应的平衡常数K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{c}_{{T}^{2}}}$ | |
| B. | 温度T℃时,混合气体的密度不变即达到平衡状态 | |
| C. | 曲线b对应的条件改变可能是加入了催化剂 | |
| D. | 若曲线b改变的条件是温度,则该正反应放热 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作 | 现象 | 结论 |
| A | C2H4通入溴水中 | 溶液褪色 | C2H4跟Br2发生加成反应 |
| B | 向溶液X中滴入NaHCO3溶液 | 产生无色气体 | X中的溶质一定是酸 |
| C | Cl2通入品红溶液中 | 溶液褪色 | Cl2具有漂白性 |
| D | 分别向0.1mol•L-1醋酸和饱和硼酸溶液中滴加 0.1mol•L-1Na2CO3溶液 | 醋酸中有气泡产生, 硼酸中没有气泡产生 | 酸性:醋酸>碳酸>硼酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥ | B. | ①⑤⑥ | C. | ②④⑥ | D. | ⑤⑥⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com