
| A. | 水蒸气通过灼热的铁粉生成氢氧化铁和氢气 | |
| B. | Mg比Al活泼,更易与NaOH溶液反应生成H2 | |
| C. | Na在空气中长期放置最终变为Na2CO3粉末 | |
| D. | 向KClO3溶液中滴加AgNO3溶液得到白色AgCl沉淀 |
分析 A.水蒸气和铁反应生成四氧化三铁和氢气;
B.Al能和NaOH溶液反应但Mg不反应;
C.Na在空气中长期放置,最终变为碳酸钠粉末;
D.氯酸钾中不含氯离子.
解答 解:A.水蒸气和铁反应生成四氧化三铁和氢气而不是氢氧化铁和氢气,故A错误;
B.Al能和NaOH溶液反应但Mg不反应,Al和NaOH溶液反应生成偏铝酸钠和氢气,故B错误;
C.Na的性质活泼,易与空气中氧气反应生成Na2O,Na2O易与水反应生成NaOH,NaOH吸收空气中的水和CO2生成Na2CO3•xH2O,Na2CO3•xH2O风化脱水生成Na2CO3,故C正确;
D.氯酸钾中不含氯离子,所以氯酸钾和硝酸银混合得不到AgCl白色沉淀,故D错误;
故选C.
点评 本题考查元素化合物性质,为高频考点,明确元素化合物性质及物质之间的转化是解本题关键,注意水蒸气和Fe反应产物成分,题目难度不大.


科目:高中化学 来源: 题型:解答题
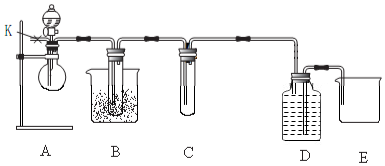
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
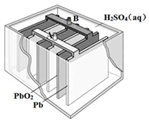 铅蓄电池是最常见的二次电池,其构造示意图如下.发生反应的化学方程式为:
铅蓄电池是最常见的二次电池,其构造示意图如下.发生反应的化学方程式为:| A. | 放电时,电解质溶液的PH值增大 | |
| B. | 放电时,电路中转移0.2mol电子时Pb电极质量减少20.7g | |
| C. | 放电时,溶液中H+向PbO2电极移动 | |
| D. | 放电时,正极反应为:PbO2(s)+4H+(aq)+SO42-(aq)+2e-═PbSO4(s)+2H2O(l) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱用于制造玻璃 | B. | 医药上用小苏打治疗胃酸过多 | ||
| C. | 打磨磁石制指南针 | D. | 工业上利用合成氨实现人工固氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
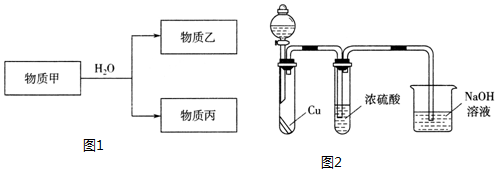
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酶是具有催化功能的蛋白质 | |
| B. | 酶的催化作用具有选择性和专一性 | |
| C. | 高温或紫外线的照射会降低酶的活性 | |
| D. | 酶通常在强酸或强碱的条件下发挥作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 s(秒)时B的浓度为0.3 mol•L-1 | |
| B. | 4s内用物质A表示的反应速率为0.075 mol•L-1•s-1 | |
| C. | 达平衡后B的转化率为30% | |
| D. | 达平衡后若通入一定量氦气,A的转化率降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
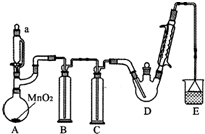 某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:
某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com