
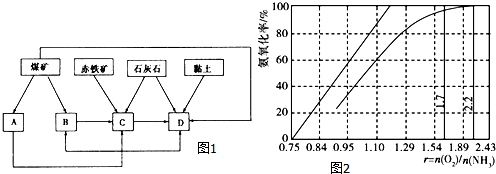
分析 (1)①煤炭燃烧可以发电,煤的干馏制造煤焦油,赤铁矿、碳酸钙是炼铁的原料,碳酸钙和黏土是生产水泥的原料;
②高炉炼铁中得到生铁的方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2、CaCO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑;
(2)①反应物投入的物质的量越多放出的热越多;
②玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料,其中玻璃纤维的作用是增强体,合成材料是基体,它的优点有:强度高、质量轻、耐腐蚀、抗冲击、绝缘性能好等;
③废旧合成材料的再生利用主要有三条途径:通过再生和改性,重新做成多种有用的材料和制品;采用热裂解或化学处理方法使其分解,用于制备多种化工原料;将废旧的聚合物作为燃料回收利用热能;
(3)根据氨氧化的化学方程式来分析;根据O2浓度太少不利于NH3的转化分析.
解答 解:(1)①煤炭燃烧可以发电,A为发电厂,煤的干馏制造煤焦油,B为焦化厂,赤铁矿、碳酸钙是炼铁的原料,C为炼铁厂,碳酸钙和黏土是生产水泥的原料,D为水泥厂,
故答案为:发电厂;焦化厂;炼铁厂;水泥厂;
②高炉炼铁中得到生铁的方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,产生炉渣的方程式为CaCO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑,
故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2、CaCO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑;
(2)①苯酚和甲醛发生缩聚反应,反应有大量热放出,为防止温度过高,应向已有苯酚的反应釜中间歇性的加入甲醛,并装有散热装置,
故答案为:间歇性;散热;
②玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料,其中玻璃纤维的作用是增强体,合成材料是基体,它的优点有:强度高、质量轻、耐腐蚀、抗冲击、绝缘性能好等,
故答案为:增强体;强度高、质量轻、耐腐蚀、抗冲击、绝缘性能好;
③废旧合成材料的再生利用主要有三条途径:通过再生和改性,重新做成多种有用的材料和制品;采用热裂解或化学处理方法使其分解,用于制备多种化工原料;将废旧的聚合物作为燃料回收利用热能,塑料深埋很久不会腐烂,会造成白色污染,酚醛塑料不能溶于有机溶剂,
故选bc;
(3)由氨氧化的化学方程式:4NH3+5O2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$4NO+6H2O,可知氨氧化率达到100%,理论上r{n(O2)/n(NH3)}=$\frac{5}{4}$=1.25,O2浓度太少不利于NH3的转化,γ{n(O2)/n(NH3)值为2.2时NH3氧化率已近100%,
故答案为:1.25;O2太少不利于NH3的转化,r值为2.2时NH3氧化率已近100%.
点评 本题考查金属冶炼,涉及到氧化还原方程式的书写,题目难度中等,本题注意从题目中获取信息,结合物质的性质解答.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 分子式符合CnH2n+2的烃一定是烷烃 | |
| B. | 烷烃均能与氯水发生取代反应 | |
| C. | 正戊烷的熔沸点比乙烷的高 | |
| D. | 烷烃不能被酸性高锰酸钾等强氧化剂氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LBr2通入足量的NaOH溶液中生成NaBr和NaBrO,则转移电子数为0.5NA | |
| B. | 5.6gFe溶于1L0.3moL/L硝酸中,转移的电子数为0,3NA | |
| C. | 足量的Zn与浓硫酸共热可生成标准状况下的气体2.24L,则参加反应的硫酸为0.4NA | |
| D. | 标准状况下,11.2LN2和H2的混合气体中所含原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 和
和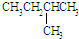
 和
和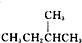
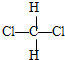 和
和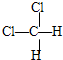
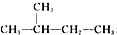 和
和
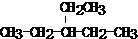 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于1.06 g | B. | 大于1.06 g而小于2.86 g | ||
| C. | 等于2.86 g | D. | 大于2.86 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 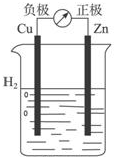 稀H2SO4Cu-Zn原电池 | |
| B. | 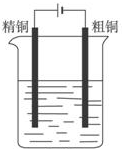 CuSO4粗铜的精炼 | |
| C. | 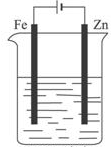 ZnCl2溶液铁片镀锌 | |
| D. | 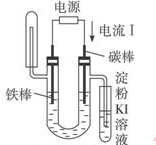 饱和氯化钠溶液验证NaCl溶液(含酚酞)电解产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20Ne和22Ne互为同位素 | B. | 20Ne和22Ne的质子数为10 | ||
| C. | 20Ne和22Ne的电子数相同 | D. | 20Ne和22Ne的中子数相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com