
【题目】下列根据实验操作和现象所得出的结论不正确的是( )
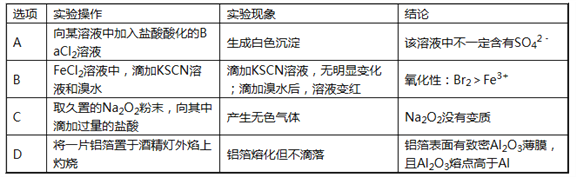
A. A B. B C. C D. D
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,属于氧化还原反应同时又是吸热反应的是
A.Ba(OH)2·8H2O与NH4Cl反应
B.铝与稀盐酸
C.灼热的炭与水蒸气生成一氧化碳和氢气的反应
D.煤与O2的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述中,正确的是( )
A.12.0 g NaHSO4晶体中阳离子和阴离子的总数为0.3NA
B.14 g分子式为CnH2n的链烃中含有的碳碳双键的数目一定为NA/n
C.标准状况下,1 L液态水中含有的H+数目为10-7NA
D.足量Zn与一定量的浓硫酸反应,产生22.4 L气体时,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造等领域。工业上以食盐、氨气(主要由合成氨厂提供)和二氧化碳为主要原料生产纯碱。其流程如下:
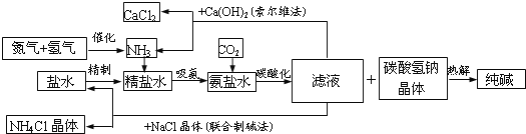
(1)盐水精制的过程是除去溶液中各种杂质的过程.为将盐水中含有的Ca2+、Mg2+等沉淀,可以向其中加入过量纯碱.此时将混合液中不溶物除去的方法是 ,该操作中所用的仪器有铁架台 (带铁圈)、 玻璃棒、烧杯等, 还需要使用的仪器有 ,溶液中多余的纯碱可以加 试剂来除去。
(2)上述工艺流程中,加压条件下通入二氧化碳进行碳酸化时没有析出碳酸钠晶体,其原因是 。整个过程中循环利用的物质是 (用化学式表示)。
(3)若采用上述流程生产106吨纯碱,则理论上通入的二氧化碳的体积(标准状况下)不得少于 L(不考虑二氧化碳的回收利用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 11.2 L H2中含有氢原子的个数为NA
B. 在标准状况下,22.4 L H2O中含有氢原子的个数为2NA
C. 32 g O3中含有氧原子的个数为2NA
D. 1 mol/L NaCl溶液中含有钠离子的个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答问题:
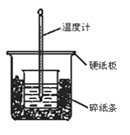
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”“偏小”“无影响”)。
(4)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”“不相等”,下同),所求中和热 ,简述理由: 。
(5)用50mL 0.50 mol·L-1醋酸代替盐酸进行上述实验,测得的中和热的数值会 。(均填“偏大”“偏小”“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)向某NaOH溶液中投入一块Al箔,先无明显现象,随后逐渐产生气泡,则产生气泡的离子反应方程式为______。
(2)实验室常用还原性Fe粉与水蒸气反应的实验来研究Fe的还原性,则该反应的化学反应方程式为______
(3)Fe(OH)2制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为______
(4)实验时制备Al(OH)3时,常用可溶性铝盐(如Al2(SO4)3与氨水反应进行制备。某课外小组在实验时不慎向Al2(SO4)3溶液中加入了过量NaOH溶液,最终并没有制出白色沉淀Al(OH)3,则该小组同学实验时发生的总离子反应方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验报告记录了如下数据,其中数据合理的是( )
A. 用pH试纸测得氯水的pH为2.1 B. 用50mL量筒量取23.00mL浓盐酸
C. 用温度计测量出酒精的沸点为78.5℃ D. 用托盘天平称量氧化铜粉末为11.70g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com