
| A. | A和B的平衡浓度之比为5:3 | B. | A和B的平衡浓度之比为2:3 | ||
| C. | x=1 | D. | x:y=2:1 |
分析 起始浓度A为5mol/L,B为3mo1/L,C的反应速率为0.5mol/(L•min),反应开始达到平衡需2min,则C的浓度变化量为0.5mol/(L•min)×2min=1mol/L,利用浓度变化量之比等于化学计量数之比计算x:y,题目中数据不能确定x、y的值,故不能确定平衡时A、B浓度之比.
解答 解:起始浓度A为5mol/L,B为3mo1/L,C的反应速率为0.5mol/(L•min),反应开始达到平衡需2min,则C的浓度变化量为0.5mol/(L•min)×2min=1mol/L,平衡时D的浓度为0.5mol/L,浓度变化量之比等于化学计量数之比,则x:y=1mol/L:0.5mol/L=2:1,题目中数据不能确定x、y的值,故不能确定平衡时A、B浓度之比,
故选:D.
点评 本题考查化学平衡的有关计算,比较基础,注意对速率规律的理解掌握与灵活应用.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
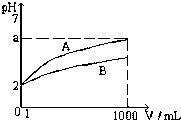 T℃时,pH=2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示
T℃时,pH=2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若X为粗铜,Y为硫酸铜,K接N,则此装置可以精炼铜 | |
| B. | 若X为铜,Y为浓硝酸,K接M,可以形成原电池,则铁为负极 | |
| C. | 若X为锌,则无论K接M还是N,铁都能被保护 | |
| D. | 若X为银,Y为FeCl3,K接N,则此装置可以在铁上镀银 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到平衡时,再充入1molX,该反应的△H变大 | |
| B. | 用Y表示4min内的反应速率为0.1mol/(L•min) | |
| C. | 再向容器中充入1molZ,达到新平衡,n(X):n(Y)=2:1 | |
| D. | 4min后,若升高温度,平衡将向逆反应方向移动,平衡常数K减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能电离出H+的化合物不一定都是酸 | B. | 2.24LO2的物质的量为0.1mol | ||
| C. | 摩尔是七个基本物理量之一 | D. | CO2的相对分子质量为44g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸、盐酸、空气和水等都是分散系 | |
| B. | 一般可用丁达尔现象区分溶液和浊液 | |
| C. | 按稳定性由弱到强的顺序排列的是溶液、胶体、浊液(以水为分散剂时) | |
| D. | 按照分散质和分散剂的状态(气、液、固态),它们之间可以有9种组合方式 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com