
| A. | ①② | B. | ①③ | C. | ②④ | D. | ①②③④ |
分析 假说法是以客观事实材料和科学理论为依据,对未知事实或规律所提出的一种推测性说明.
实验法是通过实验来验证对物质性质的预测或探究物质未知性质的方法.
分类法是指运用分类的方法,分门别类地对物质及其变化进行研究,可以总结出各类物质的通性与特性.
比较法是运用比较的方法,可以找出物质性质间的异同,认识物质间的内在联系,促进对物质性质的理解与记忆.
解答 解:①假说法是以客观事实材料和科学理论为依据,对未知事实或规律所提出的一种推测性说明,题目未提出推测性说明,故①错误;
②通过将两金属暴露于空气中,以实验研究它们在空气中的稳定性,故②正确;
③没有分门别类地对物质及其变化进行研究,故③错误;
④金属钠和铜片分别盛在表面皿中,采取对比方法来研究它们在空气中的稳定性,故④正确.
所以采取的方法为实验法、比较法.
故选C.
点评 本题考查研究物质性质及变化的基本方法,侧重考查学生的分析、实验能力,难度不大,理解常用的基本方法.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
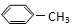 分子结构的下列叙述中,正确的是( )
分子结构的下列叙述中,正确的是( )| A. | 七个碳原子可能不在同一平面上 | B. | 具有单键和双键两种键 | ||
| C. | 八个氢原子不可能都在同一平面上 | D. | 最多可能有5个C原子在一条直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| H2(g) | Br2(g) | HBr (g) | |
| 1mol分子中的化学键断裂时需吸收的能量(KJ) | 436 | a | 369 |
| A. | 404 | B. | 260 | C. | 230 | D. | 200 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
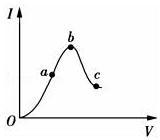 阅读下列信息,完成下列各题
阅读下列信息,完成下列各题查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食盐可作调味剂,也可作食品防腐剂 | |
| B. | 纯碱可用于清洗油污 | |
| C. | 侯式制碱法的工艺过程中应用了物质溶解度的差异 | |
| D. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2═Na2O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com