
将总物质的量为l的Na2O2和Al2(SO4)3的混合物投入足量水中,充分反应后生成y mol沉淀(y>0).若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值和y=f(x)关系式填写在表内(可不填满,也可补充).
| 序号 | x值 | y=f(x) |
| ① | 0<x≤3 |
|
| ② | 3<x<3.2 |
|
| ③ |
|
|
| ④ |
|
|
| 有关混合物反应的计算. | ||||||||||
| 分析: | Na2O2和与H2O反应生成的NaOH,恰好与Al2(SO4)3反应时,生成的Al(OH)3沉淀量最大.根据反应式知道此时,n(Na2O2):n[Al2(SO4)3]=3:1, 当n(Na2O2):n[Al2(SO4)3]≤3:1时,NaOH不足(或恰好反应),与Al3+反应生成Al(OH)3,由Na2O2根据Na原子守恒计算NaOH的物质的量,根据OH﹣守恒由NaOH计算Al(OH)3沉淀的量. 当n(Na2O2):n[Al2(SO4)3]>3:1时,Al的存在有Al(OH)3和AlO2﹣两种,有XmolNa2O2,则Al2(SO4)3为(4﹣X)mol,由Na2O2根据Na原子守恒计算NaOH的物质的量,Na2O2和与H2O反应生成的NaOH有两部分作用,(一)与Al3+反应生成Al(OH)3,(二)与Al3+反应生成AlO2﹣,根据Al原子守恒用x、y表示出AlO2﹣,的物质的量,进而表示出上述两部分消耗的NaOH的量,两部分消耗的NaOH的物质的量之和即为Na2O2和与H2O反应生成的NaOH. | |||||||||
| 解答: | 解:设Na2O2为xmol,则Al2(SO4)3为(4﹣x)mol, 据Na原子守恒得n(NaOH)=2n(Na2O2)=2xmol, 根据Al原子守恒得n(Al3+)=2n[Al2(SO4)3]=2(4﹣x)mol, Na2O2和与H2O反应生成的NaOH,恰好与Al2(SO4)3反应时,生成的Al(OH)3沉淀量最大,所以有n(Al3+):n(NaOH)=1:3,即2(4﹣x)mol:2Xmol=1:3,解得,X=3,所以(4﹣x)mol=1mol,即n(Na2O2):n[Al2(SO4)3]=3:1. 当n(Na2O2):n[Al2(SO4)3]≤3:1时,NaOH不足,根据NaOH计算Al(OH)3的量,根据OH﹣守恒有2x=3y,即y=x. 由于n(Na2O2):n[Al2(SO4)3]≤3:1,y>0;所以Xmol:(4x)mol≤3:1, x>0,联立解得,0<x≤3. 当n(Na2O2):n[Al2(SO4)3]>3:1时,Al的存在有Al(OH)3和AlO2﹣两种,有xmolNa2O2, 则Al2(SO4)3为(4﹣x)mol, 据Na原子守恒得n(NaOH)=2n(Na2O2)=2xmol, 根据Al原子守恒得n(AlO2﹣)=[2(4﹣x)﹣y]mol=(8﹣2x﹣y)mol,由关系式 Al3+﹣﹣3OH﹣﹣﹣Al(OH)3 ; Al3+﹣﹣4OH﹣﹣﹣AlO2﹣; 3ymol ymol 4(8﹣2x﹣y)mol (8﹣2x﹣y)mol 所以,3ymol+4(8﹣2x﹣y)mol=2xmol, 解得,y=32﹣10x 由于n(Na2O2):n[Al2(SO4)3]>3:1,Y>0;所以xmol:(4﹣x)mol>3:1,32﹣10x>0,联立解得,3<x<3.2. 故答案为:
. | |||||||||
| 点评: | 本题以过氧化钠的性质、铝的化合物性质为载体,考查范围讨论计算,难度较大,关键在于清楚反应过程,确定恰好反应点,以此分段讨论. |


科目:高中化学 来源: 题型:
下列事实与氢键有关的是( )
A.水加热到很高的温度都难以分解
B.水结成冰体积膨胀,密度变小
C.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高
D.HF、HCl、HBr、HI的热稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
(1)工业上常用高浓度的K2CO3 溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如下:
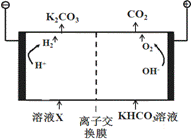
在阳极区发生的反应包括 和H ++ HCO3- == H2O + CO2↑。
(2)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。
已知:25 ℃,101 KPa下:
H2(g) + 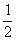 O2(g) === H2O(g) Δ H1= —242 kJ·mol-1
O2(g) === H2O(g) Δ H1= —242 kJ·mol-1
CH3OH(g) + O2(g) === CO2 (g) + 2 H2O(g) Δ H2= —676 kJ·mol-1
O2(g) === CO2 (g) + 2 H2O(g) Δ H2= —676 kJ·mol-1
① 写出CO2和H2生成气态甲醇等产物的热化学方程式 。
② 下面表示合成甲醇的反应的能量变化示意图,其中正确的是 (填字母序号)。
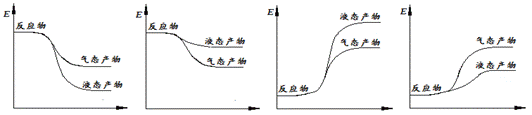
a b c d
(3)微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:

①该电池外电路电子的流动方向为 (填写“从A到B”或“从B到A”)。
②A电极附近甲醇发生的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑,对于该反应,下列判断正确的是( )
|
| A. | NaN3中氮元素的化合价为﹣3 |
|
| B. | 氧化剂和还原剂是同一物质 |
|
| C. | 反应过程中若转移1mol电子,则产生2.24L气体(标准状况) |
|
| D. | 被氧化的氮原子与生成的氮气分子个数之比为15:8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
20g烧碱配制成 500mL溶液,其物质的量浓度为 mol•L﹣1;从中取出1mL,其中含溶质为 g.若将这1mL溶液用水稀释到100mL,所得溶液中含Na+ g.
查看答案和解析>>
科目:高中化学 来源: 题型:
格林尼亚试剂简称“格氏试剂”,它是卤代烃与金属镁在无水乙醚中作用得到的,如CH3CH2Br+Mg CH3CH2MgBr,它可与羰基发生加成反应,其中的“—MgBr”部分加到羰基的氧上,所得产物经水解可得醇。今欲通过上述反应合成2丙醇,选用的有机原料正确的一组是( )
CH3CH2MgBr,它可与羰基发生加成反应,其中的“—MgBr”部分加到羰基的氧上,所得产物经水解可得醇。今欲通过上述反应合成2丙醇,选用的有机原料正确的一组是( )
A.氯乙烷和甲醛 B.氯乙烷和丙醛
C.一氯甲烷和丙酮 D.一氯甲烷和乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B两种有机物的最简式均为CH2O,下列关于它们的叙述中,正确的是( )
A.它们互为同系物
B.它们互为同分异构体
C.它们燃烧后产生的CO2和H2O物质的量之比为1:1
D.取等物质的量的A、B,完全燃烧后所消耗的O2的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”,关于标有“+”的接线柱,下列说法中正确的是( )
A.充电时作阳极,放电时作正极
B.充电时作阳极,放电时作负极
C.充电时作阴极,放电时作负极
D.充电时作阴极,放电时作正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com