
【题目】用下图中的简易装置可以进行气体的发生和收集。

(1)实验前应如何检查该装置的气密性?
(2)拨开试管a的橡皮塞,加入10ml6mol·L-1稀HNO3和1g薄铜片,立即将带有导管的橡皮塞塞紧试管口,反应开始时速度缓慢,逐渐加快,请写出试管a中所发生的所有反应的方程式。
(3)从反应开始到反应结束,预期试管a中可观察到哪些现象?请依次逐一写出。
(4)在反应开始时,可观察到导管b中的水面先沿导管b慢慢上升到一定高度,此后又回落,然后有气泡从管口冒出。试说明反应开始时,导管中水面先上升的原因。
(5)试管c收集满气体后,用拇指堵住管口,取出水槽,将管口向上,松开拇指,片刻后,再次堵住管口,将试管又再倒置于水槽中,松开拇指,此时可观察到什么现象?
【答案】(1)把导管b的下端浸入水中,用手紧握捂热试管a,导管中会有气泡冒出,松手后,水又会回升到导管b中。
(2)①3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O ②2NO+O2=2NO2 ③3NO2+H2O=2HNO3+NO
(3)①铜片和稀HNO3反应,有无色气泡产生,开始缓慢后来加快
②试管上部气体由无色变为浅棕色,又变为无色
③试管a中的溶液由无色变为浅蓝色
④反应结束后,铜片全部消耗完
(4)由于反应开始时产生的NO和试管a上部空气中的O2作用生成NO2,而NO2又易溶于水并与水反应,使装置内气体的压强暂时减小,所以导管中的水面会先上升到一定高度,此后又落回。等到试管上部空气中的O2消耗完以后,NO就会从管口冒出
(5)松开拇指后NO与空气中的氧气反应:2NO+O2=2NO2,3NO2+H2O=2HNO3+NO,导致气体体积减小,液面上升,试管内气体又变为无色
【解析】
试题分析:(1)由该装置图可知,采用“微热法”检验气密性,步骤为:把导管b的下端浸入水中,用手握住试管a,若b导管口处有气泡冒出,放手后在导管b中形成一段水柱,则证明装置气密性良好;
(2)Cu和稀硝酸反应生成硝酸铜、NO和水,NO易被氧气氧化生成二氧化氮,二氧化氮溶于水生成硝酸和NO,所以涉及的反应方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO;
(3)由发生的反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O、2NO+O2=2NO2、可知,铜片逐渐变小直至消失,溶液中有无色气泡产生,该气体在试管上部变为红棕色,试管中的溶液由无色变为浅蓝色;
(4)由于反应开始时产生的NO和试管a上部空气中的O2作用生成NO2,而NO2又易溶于水并与水反应,使装置内气体的压强暂时减小,所以导管中的水面会先上升到一定高度,此后又落回。等到试管上部空气中的O2消耗完以后,NO就会从管口冒出;
(4)松开拇指后NO与空气中的氧气反应:2NO+O2=2NO2,而生成NO2,再投入水中时发生反应:3NO2+H2O=2HNO3+NO,导致气体体积减小,液面上升,试管内气体又变为无色。


科目:高中化学 来源: 题型:
【题目】(1)某烯烃,经与氢气加成反应可得到结构简式为
的烷烃,则此烯烃可能的结构简式是:___________、___________、___________。
(2)某烃A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢。
①用系统命名法给A命名: 。
②A中的碳原子是否都处于同一平面? (填“是”或者“不是”)。
(3)有A、B、C、D、E 5种烃,各取0.01 mol充分燃烧后,B、C、E所产生的二氧化碳均为448 mL(标准状况);A或D燃烧所得的二氧化碳都是前者的3倍。在镍催化剂的作用下,A、B、C都能和氢气发生加成反应,其中A 可以转化为D,B可以转变为C或E,C可以转变为E;B或C都能使高锰酸钾酸性溶液褪色,而A、D、E无此性质;在铁屑存在时A与溴发生取代反应。
①写出烃的结构简式:B是___________,C是___________,D是___________, E是___________。
②写出A与溴反应方程式______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期元素的离子aA2+、bB+、cC3﹣、dD﹣都具有相同的电子层结构,则下列叙述正确的是( )
A. 原子半径 A>B>D>C B. 原子序数 d>c>b>a
C. 离子半径 C>D>B>A D. 单质的还原性 A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(NH4)2SO4是常见的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
【查阅资料】(NH4)2SO4在260℃和400℃时分解产物不同。
【实验探究】该小组拟选用下图所示装置进行实验(夹持和加热装置略)。

实验1:连接装置A-B-C-D,检查气密性,按图示加入试剂(装置B盛0.5000mol/L盐酸70.00mL)。通入N2排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停止通入N2。品红溶液不褪色,取下装置B,加入指示剂,用0.2000mol/LNaOH溶液滴定剩余盐酸,终点时消耗NaOH溶液25.00ml。经检验滴定后的溶液中无SO42-。
(1)仪器X的名称是 。
(2)滴定前,下列操作的正确顺序是 (填字母编号)。
a.盛装0.2000mol/LNaOH溶液
b.用0.2000mol/LNaOH溶液润洗
c.读数、记录
d.查漏、清洗
e.排尽滴定管尖嘴的气泡并调整液面
(3)装置B内溶液吸收气体的物质的量是 mol。
实验2:连接装置A-D-B,检查气密性,按图示重新加入试剂。通入N2排尽空气后,于400℃加热装置A至(NH4)2SO4完全分解无残留物,停止加热,冷却,停止通入N2。观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。进一步研究发现,气体产物中无氮氧化物。
(4)检验装置D内溶液中有SO32-,无SO42-的实验操作和现象是 。
(5)装置B内溶液吸收的气体是 。
(6)(NH4)2SO4在400℃分解的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.常温下铁与浓硫酸反应:Fe+2H+=Fe2++H2↑
B.碳酸氢钠溶液与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O
C.氯化钙溶液与碳酸氢钾溶液混合:Ca2++CO32-=CaCO3↓
D.CuSO4溶液与Ba(OH)2溶液混合:Cu2++SO42-+2OH-+Ba2+=BaSO4↓+Cu(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH—=IO3—+5I—+3H2O 下列说法不正确的是( )

A.右侧发生的电极方程式:2H2O+2e— =H2↑+2OH—
B.电解结束时,右侧溶液中含有IO3—
C.如果用阳离子交换膜代替阴离子交换膜,电解槽内
发生的总化学方程式不变
D.电解槽内发生反应的总化学方程式KI+3H2O==KIO3+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下在2L的密闭容器中充入2molSO2和2molO2,发生反应: 2SO2(g)+O2(g) ![]() 2SO3(g),进行到4min时,测得n(SO2)=1.2mol。下列说法正确的是( )
2SO3(g),进行到4min时,测得n(SO2)=1.2mol。下列说法正确的是( )
A.反应进行到2min时,容器中n(SO3)可能为0.5mol
B.当v(SO2):v(O2):v(S03)=2:1:2 时该反应达平衡状态
C.温度升高时正反应速率增大,逆反应速率减小
D.4min内氧气的平均反应速率为0.5mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
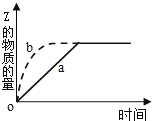
【题目】如图曲线a表示可逆反应X(g)+Y(g)Z(g)+M(g).进行过程中Z的物质的量随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
A.压缩反应容器的体积
B.加入一定量的Z
C.降低温度
D.减少X的投入量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮可以形成多种离子,如N3﹣,NH2﹣,N3﹣,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似
于NH4+,因此有类似于 NH4+的性质.
(1)写出N2H62+在碱性溶液中反应的离子方程式 .
(2)NH2﹣的电子式为 .
(3)N3﹣有 个电子.
(4)写出二种由多个原子组成的含有与N3﹣电子数相同的物质的化学式 .
(5)等电子数的微粒往往具有相似的结构,试预测N3﹣的构型 .
(6)据报道,美国科学家卡尔克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”.迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形.如果5个N结合后都达到8电子结构,且含有2个N≡N键.则“N5”分子碎片所带电荷是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com