
【题目】研究处理NOx、SO2,对环境保护有着重要的意义。回答下列问题:
(1)SO2的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的SO2。已知吸收过程中相关反应的热化学方程式如下:① SO2(g) + NH3H2O(aq) =NH4HSO3(aq) △H1 = a kJmol-1;② NH3H2O(aq) + NH4HSO3(aq) =(NH4)2SO3(aq) + H2O(l)△H2 = b kJmol-1;③ 2(NH4)2SO3(aq) + O2(g) =2(NH4)2SO4(aq) △H3= c kJmol-1,则反应 2SO2(g) + 4NH3H2O(aq) + O2(g) =2(NH4)2SO4(aq) + 2H2O(l) △H = ______。
(2)NOx的排放主要来自于汽车尾气,有人利用反应C (s) + 2NO(g)![]() N2(g) + CO2(g) △H=-34.0 kJmol-1,用活性炭对NO进行吸附。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率 α(NO)随温度的变化如图所示:
N2(g) + CO2(g) △H=-34.0 kJmol-1,用活性炭对NO进行吸附。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率 α(NO)随温度的变化如图所示:
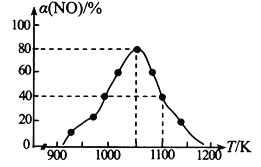
①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是_________________________; 在1100K 时,CO2的体积分数为______。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa 时,该反应的化学平衡常数Kp=________(已知:气体分压=气体总压×体积分数)。
(3)在高效催化剂的作用下用CH4还原NO2,也可消除氮氧化物的污染。在相同条件下,选用A、B、C三种不同催化剂进行反应,生成 N2的物质的量与时间变化关系如图所示,其中活化能最小的是_________(填字母标号)。

(4)在汽车尾气的净化装置中 CO和NO发生反应:2NO(g) + 2CO(g)![]() N2(g) + 2CO2(g) △H2 =-746.8 kJmol-1。实验测得,υ正=k正c2(NO) c2(CO) ,υ逆=k逆c(N2) c2(CO2) (k正、k逆为速率常数,只与温度有关)。
N2(g) + 2CO2(g) △H2 =-746.8 kJmol-1。实验测得,υ正=k正c2(NO) c2(CO) ,υ逆=k逆c(N2) c2(CO2) (k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数_____(填" >”、“< ”或“=”) k逆增大的倍数。
②若在1L 的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则![]() =_____(保留2位有效数字)。
=_____(保留2位有效数字)。
【答案】(2a+2b+c)kJmol-1 1050K前反应未达到平衡状态,随着温度升高,反应速率加快,NO转化率增大 20% 4 A < 0.25
【解析】
(1)利用盖斯定律解答。
(2)①在1050K前反应未达到平衡状态,随着温度升高,反应速率加快,NO转化率增大;达到平衡后,升高温度,平衡左移,NO的转化率降低。恒温恒压下体积分数等于物质的量分数。
②利用化学平衡常数表达式计算。
(3)A反应速率快,先达到平衡,故活化能最小。
(4)①正反应为放热反应,升高温度平衡左移,则正反应速率增大的倍数小于逆反应速率增大的倍数。
②当反应达到平衡时,υ正=υ逆,故![]() =c(N2)c2(CO2)/[c2(NO)c2(CO)]=K。
=c(N2)c2(CO2)/[c2(NO)c2(CO)]=K。
(1)① SO2(g) + NH3H2O(aq) =NH4HSO3(aq) △H1 = a kJmol-1;
② NH3H2O(aq) + NH4HSO3(aq) =(NH4)2SO3(aq) + H2O(l)△H2 = b kJmol-1;
③ 2(NH4)2SO3(aq) + O2(g) =2(NH4)2SO4(aq) △H3= c kJmol-1;
利用盖斯定律,将①×2+②×2+③可得2SO2(g) + 4NH3H2O(aq) + O2(g) = 2(NH4)2SO4(aq) + 2H2O(l)的△H =(2a+2b+c)kJmol-1,故答案为:(2a+2b+c)kJmol-1。
(2)①在1050K前反应未达到平衡状态,随着温度升高,反应速率加快,NO转化率增大;达到平衡后,升高温度,平衡左移,NO的转化率降低。根据反应C (s) + 2NO(g)![]() N2(g) + CO2(g),假设加入1molNO,在1100K时,NO的转化率为40%,则△n(NO)=0.4mol,故n(CO2)=0.2mol,由于反应前后气体的总物质的量不变,故混合气体中CO2的体积分数为
N2(g) + CO2(g),假设加入1molNO,在1100K时,NO的转化率为40%,则△n(NO)=0.4mol,故n(CO2)=0.2mol,由于反应前后气体的总物质的量不变,故混合气体中CO2的体积分数为![]() %=20%,故答案为:1050K前反应未达到平衡状态,随着温度升高,反应速率加快,NO转化率增大;20%。
%=20%,故答案为:1050K前反应未达到平衡状态,随着温度升高,反应速率加快,NO转化率增大;20%。
②根据反应C (s) + 2NO(g)![]() N2(g) + CO2(g),假设加入1molNO,在1050K时, α(NO)=80%,平衡时n(NO)=0.2mol,n(N2)=0.4mol,n(CO2)=0.4mol,各物质的平衡分压p分(NO)=
N2(g) + CO2(g),假设加入1molNO,在1050K时, α(NO)=80%,平衡时n(NO)=0.2mol,n(N2)=0.4mol,n(CO2)=0.4mol,各物质的平衡分压p分(NO)=![]() Pa,p分(N2)=
Pa,p分(N2)=![]() ×1.1×106Pa,p分(CO2)=
×1.1×106Pa,p分(CO2)=![]() ×1.1×106Pa,故反应的化学平衡常数Kp=
×1.1×106Pa,故反应的化学平衡常数Kp=![]() ×1.1×106Pa×
×1.1×106Pa×![]() ×1.1×106Pa÷(
×1.1×106Pa÷(![]() Pa)2=4,故答案为:4。
Pa)2=4,故答案为:4。
(3)A反应速率快,先达到平衡,故活化能最小,故答案为:A。
(4)①正反应为放热反应,升高温度平衡左移,则正反应速率增大的倍数小于逆反应速率增大的倍数,故k正增大的倍数小于k逆增大的倍数。故答案为:<。
②当反应达到平衡时,υ正=υ逆,故![]() =c(N2)c2(CO2)/c2(NO)c2(CO)=K,根据化学方程式可知,平衡时c (NO)=c(CO)=0.6molL-1,c(N2)=0.2 molL-1,c(CO2)=0.4 molL-1,故
=c(N2)c2(CO2)/c2(NO)c2(CO)=K,根据化学方程式可知,平衡时c (NO)=c(CO)=0.6molL-1,c(N2)=0.2 molL-1,c(CO2)=0.4 molL-1,故![]() = c(N2)c2(CO2)/[c2(NO)c2(CO)]=(0.2×0.42)/(0.62×0.62)=20/81≈0.25,故答案为:0.25。
= c(N2)c2(CO2)/[c2(NO)c2(CO)]=(0.2×0.42)/(0.62×0.62)=20/81≈0.25,故答案为:0.25。


科目:高中化学 来源: 题型:
【题目】I.迷迭香酸(F)的结构简式为: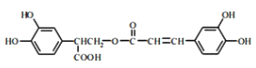 (该分子中的酚羟基有酸性,可与强碱中和);它是存在于许多植物中的一种多酚,具有抗氧化、延缓衰老、减肥降脂等功效,以A为原料合成F的路线如下:
(该分子中的酚羟基有酸性,可与强碱中和);它是存在于许多植物中的一种多酚,具有抗氧化、延缓衰老、减肥降脂等功效,以A为原料合成F的路线如下:

根据题意回答下列问题:
(1)迷迭香酸(F)的中无氧官能团为________________(填写名称)。写出结构简式:A________________;D________________。
(2)写出反应类型:反应①________________;反应②________________。
(3)反应③的试剂:________________________。
(4)1mol F与NaOH溶液反应,最多可消耗NaOH________mol。
(5)写出E与乙醇生成酯的化学反应方程式。___________________________________
II.乳酸![]() 有很强的防腐保鲜功效,可用在果酒、饮料、肉类等的保存,起到调节pH值、抑菌、延长保质期、调味、保持食品色泽、提高产品质量等作用。
有很强的防腐保鲜功效,可用在果酒、饮料、肉类等的保存,起到调节pH值、抑菌、延长保质期、调味、保持食品色泽、提高产品质量等作用。
(1)试写出以丙烯(CH2=CHCH3)为原料,合成乳酸的路线流程图(无机试剂任选)。(合成路线常用的表示方式为:甲![]() 乙……
乙……![]() 目标产物)______________
目标产物)______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,可逆反应:A2(g)+B2(g)![]() 2AB(g),达到平衡的标志是( )
2AB(g),达到平衡的标志是( )
A.容器的总压强不随时间而变化
B.单位时间内生成nmolA2同时就有2nmolAB生成
C.单位时间内有nmolB2发生反应的同时有nmolAB分解
D.单位时间内有nmolA2生成的同时有nmolB2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇脱水是制取烯烃的常用方法,实验室以环己醇为原料制取环己烯的实验装置如图所示。
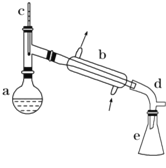
反应的化学方程式:
合成反应:
在a中加入40g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中,分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯20g。
可能用到的有关数据如下:
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
回答下列问题:
(1)装置b的名称是___________
(2)加入碎瓷片的作用是_________
(3)本实验中最容易产生的副反应的化学方程式为______________
(4)分离提纯过程中加入无水氯化钙的目的是________________
(5)本实验所得到的环己烯产率是____(填正确答案标号)
A.41% B.50% C.61% D.70%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应Zn+H2SO4===ZnSO4+H2↑,下列叙述正确的是( )

A. 反应过程中的能量关系可用上图表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若将其设计为原电池,则锌作正极
D. 若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酶在生命活动和工业生产中都有很好的催化效果。有下列物质的转化关系:

请回答:
(1)E→F 的反应类型_______________;
(2)有机物 B、 C 都含有的官能团名称___________________;
(3)写出 C 与 F 在浓硫酸加热条件下发生反应的化学方程式__________________;
(4)写出C在一定条件下发生缩聚反应生成产物的结构简式____________________;
(5)写出与G含有相同官能团且能发生银镜反应的一种同分异构体______________;
(6)下列说法正确的是_______。
A.可以用 NaOH 溶液鉴别物质 B、C、D
B.等物质的量的C 和 D 分别与足量的钠反应,产生等物质的量的氢气
C.葡萄糖和E均可以发生银镜反应
D. 物质 F 一定条件下可以转化为 E,E也可以转化为D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国Lawrece Liermore国家实验室(LINL)成功地在高压下将![]() 转化为具有类似
转化为具有类似![]() 结构的原子晶体,下列关于
结构的原子晶体,下列关于![]() 的原子晶体说法,正确的是:
的原子晶体说法,正确的是:
A. ![]() 的原子晶体和分子晶体互为同分异构体
的原子晶体和分子晶体互为同分异构体
B. 在一定条件下,![]() 原子晶体转化为
原子晶体转化为![]() 分子晶体是物理变化
分子晶体是物理变化
C. ![]() 的原子晶体和
的原子晶体和![]() 分子晶体具有相同的物理性质和化学性质
分子晶体具有相同的物理性质和化学性质
D. 在![]() 的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合
的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲测定金属镁的相对原子质量,请利用下图给定的仪器组成一套实验装置(每个仪器只能使用一次,假设气体的体积可看作标准状况下的体积)。

填写下列各项(气流从左到右):
(1)各种仪器连接的先后顺序是__________接________、________接________、________接________、________接________(用小写字母表示)。
(2)连接好仪器后,要进行的操作有以下几步,其先后顺序是________________(填序号)。
①待仪器B中的温度恢复至室温时,测得量筒C中水的体积为Va mL;
②擦掉镁条表面的氧化膜,将其置于天平上称量,得质量为m g,并将其投入试管B中的带孔隔板上;
③检查装置的气密性;
④旋开装置A上分液漏斗的活塞,使其水顺利流下,当镁完全溶解时再关闭这个活塞,这时A中共放入水Vb mL。
(3)根据实验数据可算出金属镁的相对原子质量,其数学表达式为___________________。
(4)若试管B的温度未冷却至室温,就读出量筒C中水的体积,这将会使所测定镁的相对原子质量数据________(填“偏大”“偏小”或“无影响”)。
(5)仔细分析上述实验装置后,经讨论认为结果会有误差,于是又设计了如下图所示的实验装置。

①装置中导管a的作用是_________________________________________。
②实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则产生氢气的体积为____________mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com