


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、服用铬含量超标的药用胶囊,会对人体健康造成危害 |
| B、血液透析是利用了胶体的性质 |
| C、绿色化学的核心是应用化学原理对环境污染进行治理 |
| D、在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| B、在食盐溶液蒸发结晶的过程中,当蒸发皿中出现较多量固体时即停止加热 |
| C、先在天平两个托盘上各放一张相同质量的纸,再把氢氧化钠固体放在纸上称量 |
| D、过滤时,慢慢地将液体直接倒入过滤器中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全部都是 | B、①②③⑤⑥ |
| C、①②③④⑤ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液pH=4 |
| B、由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
| C、此酸的电离平衡常数约为1×10-7 mol?L-1 |
| D、升高温度,溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
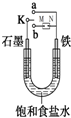 如图所示:
如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| ①5种阳离子为:Mg2+、Ba2+、Fe3+、X、Y |
| ②5种阴离子为:OH-、Cl-、CO32-、NO3-、Z |
| ③X是短周期主族元素中金属性最强的元素形成的简单阳离子;Y是简单的阳离子,具有10个电子,且离子半径是10个电子离子中最小的. |
查看答案和解析>>
科目:高中化学 来源: 题型:
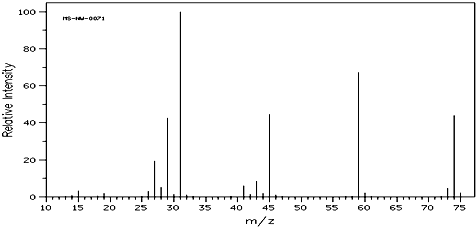
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com