
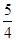 O2(g)=
O2(g)=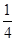 P4O10(s) △H=-738.5kJ·mol-1
P4O10(s) △H=-738.5kJ·mol-1  能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源:不详 题型:单选题
| A.S(s)+O2(g)= SO2(g);△H=-269.8kJ/mol |
| B.中和热的热化学方程式:NaOH(aq)+HCl(aq)= NaCl(aq)+H2O(l);△H=+57.3kJ/mol |
| C.燃烧热的热化学方程式: C2H5OH(l)+3O2(g)= 2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol |
| D.2NO2 = O2+2NO;△H = +116.2kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
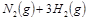
 2NH3(g))在工业生产中的大量运用,满足了人口的急剧增长对粮食的需求,也为化工生产提供了足够的原料。按要求回答下列问题:
2NH3(g))在工业生产中的大量运用,满足了人口的急剧增长对粮食的需求,也为化工生产提供了足够的原料。按要求回答下列问题: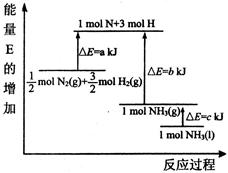
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H 0(填“>”、“<”、
C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H 0(填“>”、“<”、

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
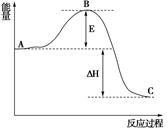
 。
。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由于红磷转化为白磷是放热反应,等质量的红磷能量比白磷低 |
| B.稀硫酸与稀NaOH溶液反应的中和热△H=57.3 kJ/mol |
| C.碳的燃烧热大于-110.5 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,△H 大于 -57.3 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g);△H =" a" kJ/mol,反应过程的能量变化如图所示。已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ。请回答:
2SO3(g);△H =" a" kJ/mol,反应过程的能量变化如图所示。已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ。请回答: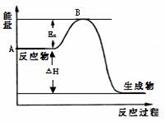
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com