
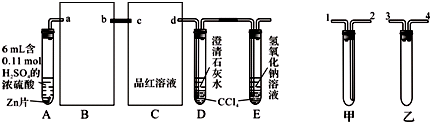
分析 (1)B的作用是防止倒吸;C装置的作用是检验二氧化硫的漂白性,可用洗气装置; 乙可防止倒吸;
(2)浓硫酸与锌反应生成硫酸锌、二氧化硫气体和水,有二氧化硫生成能证明浓硫酸具有强氧化性;
(3)随反应进行浓H2SO4变成稀H2SO4,锌与稀硫酸反应生成氢气.
解答 解:(1)B的作用是防止倒吸,可将乙填入B中;C装置的作用是检验二氧化硫的漂白性,可用洗气装置,可将甲填入C中,且为长进短出,DE中的四氯化碳可以防止气体吸收时倒吸;
故答案为:3(或4);4(或3); 2; 1;防止倒吸;
(2)浓硫酸与锌反应的化学方程式为:Zn+2H2SO4=ZnSO4+SO2↑+2H2O,有二氧化硫生成能证明浓硫酸具有强氧化性,二氧化硫能使品红褪色,
故答案为:C中品红溶液褪色;Zn+2H2SO4=ZnSO4+SO2↑+2H2O;
(3)随反应的进行浓H2SO4变成稀H2SO4,稀硫酸与Zn反应放出H2,所以生成气泡量又会明显增加,
故答案为:浓H2SO4变成稀H2SO4,稀硫酸与Zn反应放出H2.
点评 本题考查了浓硫酸的性质、二氧化硫的检验方法,题目难度中等,注意掌握铜与浓硫酸的反应原理,本题中注意锌能够浓硫酸、稀硫酸反应,明确实验目的及基本操作方法为解答关键.


科目:高中化学 来源: 题型:选择题
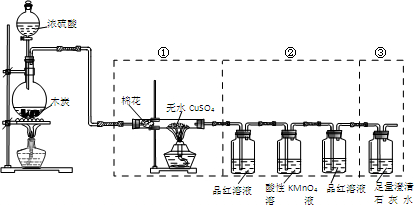
| A. | 实验时可观察到装置①中白色硫酸铜粉末变蓝色 | |
| B. | 装置②中前后两次观察到品红溶液的现象应不相同 | |
| C. | 装置③用于检验产物中二氧化碳气体的生成 | |
| D. | 如果将仪器的连接顺序变为②③①,同样可以检出所有气体产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质 | A | NaCl | KCl | CaCl2 |
| 熔点(K) | 1074 | 918 | ||
| 物质 | B | Na | Mg | Al |
| 熔点(K) | 317 | 923 | 933 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与Al反应放出H2的溶液:Mg2+、Ca2+、HCO3-、NO3- | |
| B. | 10mol•L-1的浓氨水:Al3+、NH4+、NO3-、I- | |
| C. | 0.1mol•L-1KMnO4溶液:Na+、Fe2+、SO42-、Cl- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液K+、Na+、AlO2-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com