
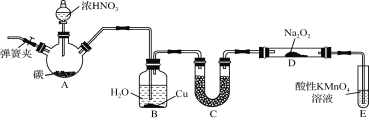
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量。某兴趣小组用下图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去)。
【背景素材】
①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4氧化成NO![]() ,MnO
,MnO![]() 被还原为Mn2+。
被还原为Mn2+。
③在酸性条件下NaNO2能把I-氧化为I2;S2O32-能把I2还原为I-。
【制备NaNO2】
(1) 装置A三颈烧瓶中发生反应的化学方程式为 。
(2) B装置的目的是① ,② 。
(3) 为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是 (填序号)。
A. P2O5 B. 碱石灰 C. 无水CaCl2 D. 生石灰
(4) E装置发生反应的离子方程式是 。
【测定NaNO2纯度】
(5) 本小题可供选择的试剂有:
A.稀硫酸
B.c1mol·L-1KI溶液
C.淀粉溶液
D.c2mol·L-1Na2S2O3溶液
E.c3mol·L-1酸性KMnO4溶液
①利用NaNO2的还原性来测定其纯度,可选择的试剂是 (填序号)。
②利用NaNO2的氧化性来测定其纯度的步骤是:准确称取质量为m g的NaNO2样品放入锥形瓶中,加适量水溶解 (请补充完整实验步骤)。
【答案】
(1)C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
(2)①将NO2转化为NO;②铜与稀硝酸反应生成NO
(3)BD;
(4)3MnO4-+4H++5NO=3Mn2++5NO3-+2H2O;
(5)①E;
②加入过量的c1mol·L-1KI溶液、淀粉溶液,然后滴加稀硫酸,充分反应后,用c2mol·L-1Na2S2O3溶液滴定至溶液由蓝色恰好变为无色,且半分钟内不变色,读数,重复以上操作2~3次。
【解析】
试题分析:(1)装置A三颈烧瓶中发生反应的化学方程式为C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)
CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(2)B装置的目的是①将NO2转化为NO、②铜与稀硝酸反应生成NO,故答案为:①将NO2转化为NO;②铜与稀硝酸反应生成NO;
(3)A、C不能吸收酸,B、D可吸收酸且干燥气体,故答案为:BD;
(4)由信息可知,E装置的作用是吸收有毒的NO气体,避免污染空气,反应的离子方程式为3MnO4- +4 H+ +5NO = 3Mn2+ + 5NO3- +2 H2O,故答案为:3MnO4- +4 H+ +5NO = 3Mn2+ + 5NO3- +2 H2O;
(5)①由信息NO能被酸性KMnO4氧化成NO3-可知,则利用NaNO2的还原性来测定其纯度,可选择的试剂是E,故答案为:E;②由信息酸性条件下NaNO2能把I-氧化为I2可知,则利用NaNO2的氧化性来测定其纯度的步骤是:准确称取质量为m的NaNO2样品放入锥形瓶中,加适量水溶解,加入过量的c1 molL-1 KI溶液、淀粉溶液,然后滴加稀硫酸,用c2 molL-1 Na2S2O3溶液滴定至溶液由蓝色恰好变为无色,且半分钟内不变色,读数,重复以上操作2~3次,故答案为:加入过量的c1 molL-1 KI溶液、淀粉溶液,然后滴加稀硫酸,用c2 molL-1 Na2S2O3溶液滴定至溶液由蓝色恰好变为无色,且半分钟内不变色,读数,重复以上操作2~3次。


科目:高中化学 来源: 题型:
【题目】以![]() 表示阿伏加德罗常数,下列说法中正确的是
表示阿伏加德罗常数,下列说法中正确的是
A.58.5 g氯化钠固体中含有![]() 个氯化钠分子
个氯化钠分子
B.1 mol Fe参与反应失去电子数目一定为2![]()
C.1 molNa被完全氧化生成Na202,失去2![]() 个电子
个电子
D.常温下,46 g N02和N204的混合物中含有的氮原子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某蛋白质由m条肽链、n个氨基酸组成。理论上该蛋白质至少含有氧原子
A. (n-m)个 B. ( n-2m)个 C. (n+m)个 D. (n+2m)个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲在金属表面镀银,应把镀件挂在电镀池的阴极。下列各组中,选用的阳极金属和电镀液均正确的是
A.Ag和AgCl溶液 B.Ag和AgNO3溶液 C.Pt和Ag2CO3溶液 D.Pt和Ag2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”——全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是( )
A.分子中三个碳原子可能处于同一直线上
B.全氟丙烷的电子式为: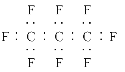
C.全氟丙烷分子中既有极性键又有非极性键的极性分子
D.相同压强下,沸点:C3F8 < C3H8
查看答案和解析>>
科目:高中化学 来源: 题型:
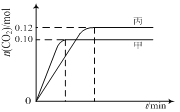
【题目】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如下图所示。下列说法正确的是( )
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如下图所示。下列说法正确的是( )
容器 | 温度/℃ | 起始物质的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
A.该反应的正反应为吸热反应
B.达到平衡时,乙中CO2的体积分数比甲中的小
C.T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆)
D.T2℃时,若起始时向丙中充入0.06mol N2和0.12 mol CO2,则达平衡时N2的转化率大于40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列哪一项不是构成蛋白质多样性的原因( )
A. 氨基酸的数目成百上千
B. 氨基酸形成肽链时,不同种类氨基酸的排列顺序千变万化
C. 肽链的盘曲、折叠方式及其形成的空间结构千差万别
D. 氨基酸的种类多达百种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L盐酸和20.00 mL 0.1000 mol/L醋酸溶液,得到2条滴定曲线,如下图所示:
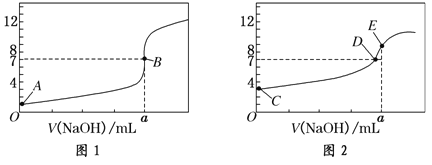
以HA表示酸,下列说法正确的是( )
A.滴定盐酸的曲线是图2
B.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A—)
C.达到B、E状态时,反应消耗的n( CH3COOH)>n(HCl)
D.当0mL< V(NaOH)<20.00mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com