
| A. | CCl4和PCl3 | B. | NaCl和HCl | C. | CO2和SiO2 | D. | NaH和Na2O2 |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键;由分子构成的晶体为分子晶体,由离子构成的晶体为离子晶体,由原子构成且存在共价键的为原子晶体,以此来解答.
解答 解:A.CCl4和PCl3都含有极性共价键,为分子晶体,故A正确;
B.NaCl为离子化合物,HCl为化合物,故B错误;
C.CO2为分子晶体,SiO2为原子晶体,故C错误;
D.NaH和Na2O2都为离子化合物,但Na2O2含有离子键和非极性共价键,故D错误.
故选A.
点评 本题考查化学键及晶体类型,为高频考点,把握化学键的形成及判断的一般规律、晶体的构成微粒及作用力为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:填空题
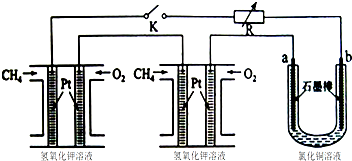
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{4}{5}$v(A)=V(B) | B. | $\frac{5}{6}$v(B)=v(D) | C. | $\frac{2}{3}$v(A)=V(D) | D. | $\frac{4}{5}$v(B)=v(C) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验事实 | 理论解释 |
| A | HCl气体溶于水,能导电 | HCl为离子化合物 |
| B | HBr的酸性强于HCl的酸性 | Br的非金属性比Cl强 |
| C | K3C60在熔融状态下能够导电 | K3C60中含有离子键 |
| D | HF的沸点高于HCl | HF分子间形成有氢键 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
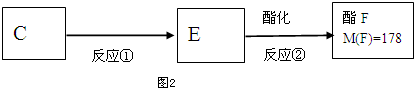
.
 ,
, ,
, .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
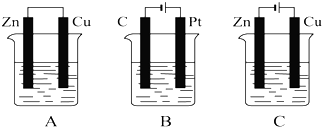
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com