
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
甲:Mg(NO3)2、NO2、O2 乙:MgO、NO2、O2
丙:Mg3N2、O2 丁:MgO、NO2、N2
(1)实验前,小组成员经讨论认定猜想丁不成立,理由是 。
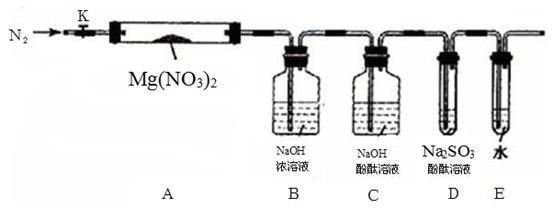
查阅资料得知:2NO2+2NaOH=NaNO3+NaNO2+H2O,针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
(2)实验过程
①取器连接后,放人固体试剂之前,关闭K,微热硬质玻璃管(A),观察到E 中有气泡连续放出,表明 。
② 称取Mg(NO3)2固体3. 79 g置于A中,加热前通人N2以驱尽装置内的空气,其目的是________;关闭K,用酒精灯加热时,正确操作是先______然后固定在管中固体部位下加热。
③ 观察到A 中有红棕色气体出现,C、D 中未见明显变化。
④ 待样品完全分解,A 装置冷却至室温、称量,测得剩余固体的质量为1.0g
⑤ 取少量剩余固体于试管中,加人适量水,未见明显现象。
(3)实验结果分析讨论
① 根据实验现象和剩余固体的质量经分析可初步确认猜想_______是正确的。
② 根据D 中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中将发生氧化还原反应 (填写化学方程式),溶液颜色会退去;小组讨论认定分解产物中有O2存在,未检侧到的原因是 。
③ 小组讨论后达成的共识是上述实验设计仍不完善,需改进装里进一步研究。
(1)不符合氧化还原反应原理
(2)①装置气密性良好
②避免对产物O2的检验产生干扰;移动酒精灯预热硬质玻璃管
(3)①乙 ②2Na2SO3+ O2 = 2Na2SO4 O2在通过装置B时已参与反应
【解析】(1)若产物是MgO、NO2 、N2。元素的化合价只有降低的没有升高的不符合氧化还原反应中化合价升高与降低的总数相等的原则。
(2)①仪器连接后,放入固体试剂之前,关闭K,微热硬质玻璃管(A),观察到E中有气泡连续放出,表明装置气密性良好,不漏气。若漏气。E中就不会观察到有连续的气泡产生。②称取Mg(NO3)2固体3.79 g置于A中,加热前通入N2以驱尽装置内的空气,其目是驱赶装置中的空气,避免空气中的成分对产物O2的检验产生干扰。关闭K,用酒精灯加热时,正确操作是先移动酒精灯预热硬质玻璃管,使之均匀受热,然后固定在管中固体部位下加热。以防受热不均匀发生爆炸事故。观察到A 中有红棕色气体出现,说明产生了NO2气体,排除了丙存在的可能。
(3)①n{Mg(NO3)2}=m/M= 3.79 g÷148g/mol=0.0256mol,n(MgO)=n(Mg)=n{Mg(NO3)2.则m(MgO)= 0.0256mol×40g/mol=1.0g
根据实验现象和剩余固体的质量经分析可初步确认猜想是乙正确的。
②若有O2,D中将发生氧化还原反应:2Na2SO3 + O2 =2Na2SO4溶液颜色会褪去;小组讨论认定分解产物中有O2存在,未检测到的原因是4NO2 + O2+ 2H2O = 4HNO3,HNO3被NaOH溶液吸收,故检测不到其存在。


科目:高中化学 来源:2014高考名师推荐化学--预测14 题型:选择题
下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是
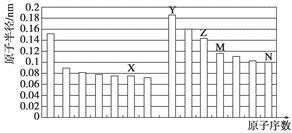
A.Z、N两种元素的离子半径相比,前者较大
B.X、N两种元素的气态氢化物的沸点相比,前者较低
C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测12 题型:选择题
下列说法不正确的是
A.已知H2(g)+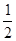 O2(g)===H2O(g) ΔH1=a kJ·mol-1;
O2(g)===H2O(g) ΔH1=a kJ·mol-1;
2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1,则a>b
B.CO的燃烧热为283.0 kJ·mol-1,则
2CO2(g)===2CO(g)+O2(g) ΔH=+566.0 kJ·mol-1
C.若N2(g)+3H2(g)  2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ
2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ
D.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和KOH反应的中和热ΔH=-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测11 题型:选择题
下列有关说法正确的是
A、氨水稀释后,溶液中 的值减小
的值减小
B、 0.1 mol·L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小
C、电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等
D、 298 K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其ΔH>0
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测11 题型:选择题
常温下,向20.00 mL 0.100 mol·L-1 CH3COONa溶液中逐滴加入0.100 0 mol·L-1盐酸,溶液的pH与所加盐酸体积的关系如下图所示(不考虑挥发)。下列说法正确的是
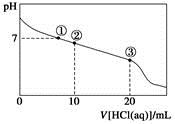
A.点①所示溶液中:c(CH3COOH)=c(Cl-)>c(OH-)=c(H+)
B.点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH)
C.点③所示溶液中:c(CH3COOH)>c(Na+)>c(H+)>c(CH3COO-)
D.整个过程中可能出现:c(H+)+c(Na+)=c(CH3COOH)+c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测10 题型:选择题
设NA表示阿伏加德罗常数的值,下列说法正确的是
A.4.0 g重水(D2O)中所含中子数为1.6 NA
B.1 L 2 mol·L-1 K2S溶液中S2-和HS-的总数为2 NA
C. 2.4g金刚石与石墨的混合物中所含碳原子数为0.2 NA
D.50 mL 18 mol·L-1浓硫酸与足量铜反应,转移的电子数为0.9 NA
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测10 题型:选择题
下列说法正确的是
A.第三周期金属元素的氧化物都属于碱性氧化物
B.电子层结构相同的不同离子,其半径随核电荷数增大而减小
C.IA族元素的金属性一定比IIA族元素的金属性强
D.单原子形成的离子,一定与稀有气体原子的核外电子排布相同
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测1 题型:选择题
25℃时,水的离子积常数为Kw,该温度下a mol?L-1的HA与bmol?L-1强碱BOH等体积混合,若恰好完全中和,下列结论中不正确的是
A.混合液中:c(H+)≤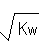
B.混合液中:c(HA)+c(A-)=amol?L-1
C.a=b
D.混合液中:c(H+)+c(B+)=c(OH-)+c(A-
查看答案和解析>>
科目:高中化学 来源:2014福建安溪一中、养正中学、惠安一中高一下学期期末化学试卷(解析版) 题型:选择题
香烟烟雾中含有CO、CO2、SO2、H2O等气体,用①无水CuSO4 ②澄清石灰水③红热CuO ④生石灰 ⑤品红溶液 ⑥酸性高锰酸钾溶液等药品可将其一一检出,检测时香烟烟雾通入药品的正确顺序是( )
A.①⑤②①④③ B.①⑤⑥②④③
C.③④②⑥⑤① D.②⑤①④③⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com