
| A. | 四氯化碳和水 | B. | 苯和汽油 | C. | 己烷与液溴 | D. | 溴丙烷和水 |
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:解答题
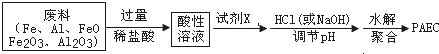
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
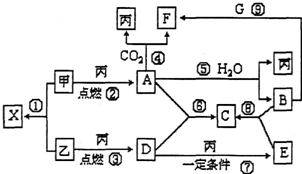 甲、乙、丙为常见单质,X、A、B、C、D、E、F、G均为常见的化合物,其中A为淡黄色固体,其摩尔质量和X相同,A、F、C、G的焰色反应都为黄色.在一定条件下,各物质间相互转化关系如图所示.
甲、乙、丙为常见单质,X、A、B、C、D、E、F、G均为常见的化合物,其中A为淡黄色固体,其摩尔质量和X相同,A、F、C、G的焰色反应都为黄色.在一定条件下,各物质间相互转化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子及其离子的核外电子层数等于该元素所在周期数 | |
| B. | 稀有气体元素原子的最外层电子数都是8 | |
| C. | 元素周期表从ⅢB到ⅡB 10个纵行的元素都是金属元素 | |
| D. | 短周期元素中,若两种元素的原子序数相差8,则它们的周期数一定相差1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 铝与稀盐酸反应 | ||
| C. | 灼热的炭与CO2反应 | D. | CO与O2燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2 | B. | HCOOCH3 | C. | CH3COOCH2CH2CH3 | D. | CH3 CH2CH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
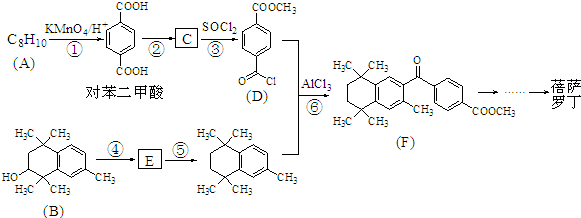
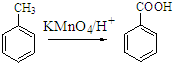
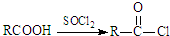
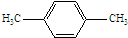 ;原料B发生反应④所需的条件为浓硫酸、加热.
;原料B发生反应④所需的条件为浓硫酸、加热.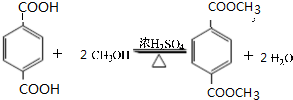 ;⑤
;⑤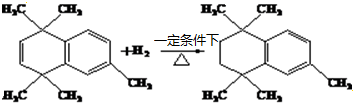 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com