
НЁіЈИЛГЗ°СІрїЄ1 molДі»ЇС§јьЛщОьКХµДДЬБїїґіЙёГ»ЇС§јьµДјьДЬЎЈјьДЬµДґуРЎїЙТФєвБї»ЇС§јьµДЗїИх,ТІїЙТФ№АЛг»ЇС§·ґУ¦µД·ґУ¦ИИ(¦¤H),»ЇС§·ґУ¦µД¦¤HµИУЪ·ґУ¦ЦР¶ПБСѕЙ»ЇС§јьµДјьДЬЦ®єНУл·ґУ¦ЦРРОіЙРВ»ЇС§јьµДјьДЬЦ®єНµДІоЎЈ
»ЇС§јь | SiЎЄO | SiЎЄCl | HЎЄH | HЎЄCl | SiЎЄSi | SiЎЄC |
јьДЬ/kJЎ¤mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
Зл»ШґрПВБРОКМв:
(1)±ИЅППВБРБЅЧйОпЦКµДИЫµгёЯµН(МоЎ°>Ў±»тЎ°<Ў±)ЎЈ
SiCЎЎЎЎЎЎЎЎSi;SiCl4ЎЎЎЎЎЎЎЎSiO2ЎЈ
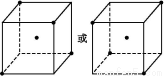
(2)ИзНјБў·ЅМеЦРРДµДЎ°Ў±±нКѕ№иѕ§МеЦРµДТ»ёцФЧУ,ЗлФЪБў·ЅМеµД¶ҐµгУГЎ°Ў±±нКѕіцУлЦ®ЅфБЪµД№иФЧУЎЈ

(3)№¤ТµЙПУГёЯґї№иїЙНЁ№эПВБР·ґУ¦ЦЖИЎ:SiCl4(g)+2H2(g) Si(s)+4HCl(g),ёГ·ґУ¦µД·ґУ¦ИИ¦¤H=ЎЎЎЎЎЎkJ/molЎЈ
Si(s)+4HCl(g),ёГ·ґУ¦µД·ґУ¦ИИ¦¤H=ЎЎЎЎЎЎkJ/molЎЈ
(1)>ЎЎ<
(2)
(3)+236
ЎѕЅвОцЎї(1)ОпЦКИЫ»ЇК±Ри¶Пјь,¶ПјьРиОьКХДЬБї,¶шјьДЬФЅґуµДОпЦК,¶ПјьЛщОьКХДЬБїФЅґу,ИЫµгФЅёЯЎЈЛщТФИЫµг:SiC>Si;SiCl4<SiO2ЎЈ
(2)ПаБЪµДЛДёц№иФЧУРОіЙХэЛДГжМеЅб№№ЎЈ
(3)1 mol№иЦРє¬2 mol SiЎЄSiјь,ФЩёщѕЭ:¦¤H=·ґУ¦ОпµДјьДЬ-ЙъіЙОпµДјьДЬ,µГ¦¤H=4E(SiЎЄCl)+2E(HЎЄH)-2E(SiЎЄSi)-4E(HЎЄCl)=4ЎБ360 kJ/mol+2ЎБ436 kJ/mol-2ЎБ176 kJ/mol-4ЎБ431 kJ/mol=+236 kJ/molЎЈ



| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а СЎРЮ3ОпЦКЅб№№УлРФЦКБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРРрКцЦРХэИ·µДКЗ(ЎЎЎЎ)
A.·ЦЧУѕ§МеЦР¶јґжФЪ№ІјЫјь
B.F2ЎўCl2ЎўBr2ЎўI2µДИЫЎў·РµгЦрЅҐЙэёЯУл·ЦЧУјдЧчУГБ¦УР№Ш
C.є¬УРј«РФјьµД»ЇєПОп·ЦЧУТ»¶ЁІ»є¬·Зј«РФјь
D.Ц»ТЄКЗАлЧУ»ЇєПОп,ЖдИЫµгТ»¶Ё±И№ІјЫ»ЇєПОпµДИЫµгёЯ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв8»ЇС§·ґУ¦ЛЩВКУл»ЇС§ЖЅєвБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
АыУГ·ґУ¦:2NO(g)+2CO(g) 2CO2(g)+N2(g)ЎЎ¦¤H =+746.8 kJЎ¤mol-1,їЙѕ»»ЇЖыіµОІЖш,Из№ыТЄН¬К±МбёЯёГ·ґУ¦µДЛЩВКєНNOµДЧЄ»ЇВК,ІЙИЎµДґлК©КЗ (ЎЎЎЎ )
2CO2(g)+N2(g)ЎЎ¦¤H =+746.8 kJЎ¤mol-1,їЙѕ»»ЇЖыіµОІЖш,Из№ыТЄН¬К±МбёЯёГ·ґУ¦µДЛЩВКєНNOµДЧЄ»ЇВК,ІЙИЎµДґлК©КЗ (ЎЎЎЎ )
A.ЅµµНОВ¶И
B.ФцґуС№ЗїН¬К±јУґЯ»ЇјБ
C.ЙэёЯОВ¶ИН¬К±ідИлN2
D.ј°К±Ѕ«CO2єНN2ґУ·ґУ¦МеПµЦРТЖЧЯ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв7ФЄЛШЦЬЖЪ±нУлФЄЛШЦЬЖЪВЙБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ФЄЛШЦЬЖЪВЙєНФЄЛШЦЬЖЪ±нКЗС§П°»ЇС§µДЦШТЄ№¤ѕЯ,ПВБРЛµ·ЁІ»ХэИ·µДКЗ(ЎЎЎЎ)
A.HFЎўHClЎўHBrЎўHIµД»№ФРФТАґОФцЗї,ИИОИ¶ЁРФТАґОјхИх
B.PЎўSЎўClµГµзЧУДЬБ¦єНЧоёЯјЫСх»ЇОп¶ФУ¦Л®»ЇОпµДЛбРФѕщТАґОФцЗї
C.µЪўсAЧеµДЅрКфµҐЦКУлЛ®·ґУ¦Т»¶Ё±ИµЪўтAЧеµДЅрКфµҐЦКѕзБТ
D.ГЕЅЭБР·тФЪЗ°ИЛ№¤ЧчµД»щґЎЙП·ўПЦБЛФЄЛШЦЬЖЪВЙ,±нГчїЖС§СРѕїјИТЄјМіРУЦТЄґґРВ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв6ФЧУЅб№№»ЇС§јьБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
№ММеAµД»ЇС§КЅОЄNH5,ЛьµДЛщУРФЧУµДЧоНвІг¶ј·ыєППаУ¦ПЎУРЖшМеФЧУµДЧоНвµзЧУІгЅб№№,ФтПВБРУР№ШЛµ·ЁІ»ХэИ·µДКЗ(ЎЎЎЎ)
A.1 mol NH5ЦРє¬УР5 NAёцNЎЄHјь(NA±нКѕ°ў·ьјУµВВЮіЈКэ)
B.NH5ЦРјИУР№ІјЫјьУЦУРАлЧУјь
C.NH5µДµзЧУКЅОЄ 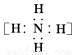 +
+
D.ЛьУлЛ®·ґУ¦µДАлЧУ·ЅіМКЅОЄNH4++H-+H2O NH3Ў¤H2O+H2Ўь
NH3Ў¤H2O+H2Ўь
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв5»ЇС§ДЬУлИИДЬБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
јЧИ©КЗТ»ЦЦЦШТЄµД»Ї№¤ІъЖ·,їЙТФАыУГјЧґјНСЗвЦЖ±ё,·ґУ¦КЅИзПВ:
ўЩCH3OH(g) CH2O(g)+H2(g)ЎЎ¦¤H1=+84.2 kJЎ¤mol-1
CH2O(g)+H2(g)ЎЎ¦¤H1=+84.2 kJЎ¤mol-1
Пт·ґУ¦МеПµЦРНЁИлСхЖш,НЁ№э·ґУ¦ўЪ2H2(g)+O2(g) 2H2O(g)ЎЎ¦¤H2=-483.6 kJЎ¤mol-1Мṩ·ґУ¦ўЩЛщРиИИБї,ТЄК№·ґУ¦ОВ¶ИО¬іЦФЪ700 Ўж,ФтЅшБПЦРјЧґјУлСхЖшµДОпЦКµДБїЦ®±ИФјОЄ(ЎЎЎЎ)
2H2O(g)ЎЎ¦¤H2=-483.6 kJЎ¤mol-1Мṩ·ґУ¦ўЩЛщРиИИБї,ТЄК№·ґУ¦ОВ¶ИО¬іЦФЪ700 Ўж,ФтЅшБПЦРјЧґјУлСхЖшµДОпЦКµДБїЦ®±ИФјОЄ(ЎЎЎЎ)
A.5.74ЎГ1B.11.48ЎГ1C.1ЎГ1D.2ЎГ1
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв4Сх»Ї»№Ф·ґУ¦Б·П°ѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
Зв»ЇСЗН(CuH)КЗТ»ЦЦДСИЬОпЦК,УГCuSO4ИЬТєєНЎ°БнТ»ОпЦКЎ±ФЪ40Ў«50 ЎжК±·ґУ¦їЙЙъіЙЛьЎЈCuHІ»ОИ¶Ё,ТЧ·ЦЅв;ФЪВИЖшЦРДЬИјЙХ;УлПЎСОЛб·ґУ¦ДЬЙъіЙЖшМе;Cu+ФЪЛбРФМхјюПВ·ўЙъµД·ґУ¦КЗ2Cu+ Cu2++CuЎЈёщѕЭТФЙПРЕПў,ЅбєПЧФјєЛщХЖОХµД»ЇС§ЦЄК¶,»Шґр:
Cu2++CuЎЈёщѕЭТФЙПРЕПў,ЅбєПЧФјєЛщХЖОХµД»ЇС§ЦЄК¶,»Шґр:
(1)УГCuSO4ИЬТєєНЎ°БнТ»ОпЦКЎ±ЦЖCuHµД·ґУ¦ЦР,УГСх»Ї»№Ф№Ыµг·ЦОц,ХвЎ°БнТ»ОпЦКЎ±ФЪ·ґУ¦ЦРЛщЖрµДЧчУГКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
(2)РґіцCuHФЪВИЖшЦРИјЙХµД»ЇС§·ґУ¦·ЅіМКЅ
(3)CuHИЬЅвФЪПЎСОЛбЦРЙъіЙµДЖшМеКЗЎЎЎЎЎЎЎЎ,Из№ы·ґУ¦ЦРЙъіЙБЛ±кЧјЧґїцПВ22.4 LµДЖшМе,±»»№ФµДАлЧУµГµзЧУµДОпЦКµДБїКЗЎЎЎЎЎЎЎЎЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв3АлЧУ·ґУ¦Б·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРёчЧйАлЧУФЪЦё¶ЁИЬТєЦРТ»¶ЁДЬґуБї№ІґжµДКЗ(ЎЎЎЎ)
A.ДЬК№јЧ»щіИіКємЙ«µДИЬТє:Ba2+ЎўAl3+ЎўNO3ЎЄЎўCl-
B.УЙЛ®µзАліцµДc(H+)=1ЎБ10-11 molЎ¤L-1µДИЬТє:Na+ЎўMg2+ЎўCl-ЎўNO3ЎЄ
C.0.2 molЎ¤L-1µДNaNO3ИЬТє:H+ЎўFe2+ЎўSO42ЎЄЎўCl-
D.УлFe·ґУ¦ЙъіЙH2µДИЬТє:NH4+ЎўK+ЎўSO42ЎЄЎўCO32ЎЄ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ГыК¦ЦЄК¶µгѕ«±а ЧЁМв21»ЇС§КµСй»щґЎБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
№ШУЪПВБРёчКµСйЧ°ЦГµДРрКцЦР,І»ХэИ·µДКЗ(ЎЎЎЎ)
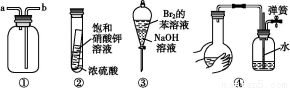
A.Ч°ЦГўЩїЙУГУЪКХјЇH2ЎўNH3ЎўCO2ЎўCl2ЎўHClЎўNO2µИЖшМе
B.КµСйўЪ·ЕЦГТ»¶ОК±јдєу,РЎКФ№ЬДЪУРѕ§МеОціц
C.КµСйўЫХсµґєуѕІЦГ,ЙПІгИЬТєСХЙ«±дЗі
D.КµСйўЬІ»ДЬУГАґјмІйЧ°ЦГµДЖшГЬРФ
Ійїґґр°ёєНЅвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com