
【题目】氮氧化铝(AlON)属原子晶体,是一种超强透明材料,可以由反应Al2O3+C+N2![]() 2AlON+CO合成,下列有关说法正确的是( )
2AlON+CO合成,下列有关说法正确的是( )
A. 氮氧化铝中氮的化合价是-3
B. 反应中氧化产物和还原产物的物质的量之比是1∶2
C. 反应中每生成5.7 g AlON同时生成1.12 L CO
D. AlON和CO的化学键类型不同
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:
【题目】镁、硼及其化合物在工农业生产中应用广泛。已知:硼、铝同主族;硼砂常指四硼酸钠的十水合物,化学式为Na2B4O7·10H2O。利用硼镁矿(主要成分为Mg2B2O5·H2O)制取金属镁及粗硼的工艺流程图如图所示:

(1)Mg2B2O5·H2O 中B的化合价为______价。
(2)操作②的主要步骤是_______________和过滤,从而获得MgCl26H2O。
(3)MgCl26H2O在HCl氛围中加热才能制得无水氯化镁。其原因是____________________;若用情性电极电解MgCl2溶液,其阴极反应式为_____________________________。
(4)硼砂溶于90℃热水后,常用稀硫酸调pH至2~3制取H3BO3晶体,该反应的离子方程式为______;X为硼酸晶体加热完全脱水后的产物,其与Mg反应制取粗硼的化学方裎式为_____________。
(5)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+=Mg2++2H2O。常温下,若起始电解质溶液pH=1,则当pH =2时,溶液中Mg2+的浓度为___________。
(6)制得的粗硼在一定条件下可反位生成BI3,BI3加热分解即可得到纯净的单质硼。现将mg粗硼制成的BI3充全分解,生成的I2用c mol L-1Na2S2O3溶液滴定至终点,三次消耗Na2S2O3溶液的体积平均值为 VmL。则该粗硼样品的纯度为___________。(提示:I2+2S2O32-=2I-+S4O62-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时.向2.0 L恒容密闭容器中充入1.0 mol PCl5,发生反应PCl5 (g)![]() PCl3(g)+Cl2(g),经过一段时间后达到平衡,反应过程中测定的部分数据列于下表。下列说法正确的是
PCl3(g)+Cl2(g),经过一段时间后达到平衡,反应过程中测定的部分数据列于下表。下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A. 在前50s,PCl3的平均反应速率 v(PCl3)=0.0032mol/(L·s)
B. 达到平衡时,容器中的压强是起始时的1.2倍
C. 相同温度下,起始时向容器中充入1.0mo PCl5、0.20 mo1 PCl3和0.20 mo1 Cl2,反应达到平衡前v(正)>v(逆)
D. 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H10的有机物,该有机物能够使酸性高锰酸钾溶液褪色,该有机物可能的结构(不考虑顺反和空间结构)有多少种( )
A. 4种 B. 5种 C. 6种 D. 7种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于碱金属元素的下列叙述中,错误的是( )
A. 碱金属元素原子最外层都只有1个电子
B. 随核电荷数递增,氢氧化物碱性增强
C. 依Li、Na、K、Rb、Cs,单质熔沸点升高,密度增大
D. 随电子层数增加,原子半径增大,金属性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,1994年12月科学家发现了一种新元素,它的原子核内有161个中子,质量数为272,该元素的原子序数为 ( )
A. 111 B. 161 C. 272 D. 433
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素在周期表中的位置如图,则下列说法错误的是

A. 若Y的最简单氢化物的沸点比M的低,则X单质可与强碱溶液反应
B. 简单阴离子半径M>Z>Y
C. 若Y的氢化物水溶液呈碱性,则X的氧化物不与任何酸反应
D. 最高价氧化物对应水化物的酸性Z>M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO4晶体易溶于水,它溶于水时,电离出三种不同的离子,电离方程式为:NaHSO4===Na+ + H+ + SO42-,因此NaHSO4溶液显酸性。但NaHSO4受热熔化时却只能电离出两种不同离子。
(1)NaHSO4在熔融状态下的电离方程式是________________。
(2)下列说法中正确的是________(填序号)。
A.NaHSO4属于酸 B.NaHSO4属于氢化物
C.NaHSO4晶体属于电解质 D.NaHSO4溶液能与Zn反应生成氢气
(3)向一定量的Ba(OH)2溶液中,逐滴加入NaHSO4溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为:_________________________________________,沉淀完全后,继续滴加NaHSO4溶液,此时发生反应的离子方程式为:_____________。
(4)NaHSO4和NaHCO3中都含有氢元素,但将二者同时加入水中,可以发生化学反应,该反应的离子方程式为:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素在元素周期表中的位置如图所示,已知:E元素原子的最外层电子数是次外层的2倍。下列说法不正确的是
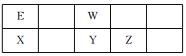
A. X有多种氢化物 B. 简单阴离子的半径:Y>Z
C. 气态氢化物的稳定性:W>Y>Z D. Y的氢化物与Z单质能发生化学反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com