
| A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定 |
| B.锥形瓶用蒸馏水洗涤后未用待测液润洗 |
| C.读取标准液读数时,滴定前平视,滴定到终点后俯视 |
| D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失 |
| A.托盘天平 | B.量筒 |
| C.碱式滴定管 | D.酸式滴定管 |
 。
。

 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源:不详 题型:单选题
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
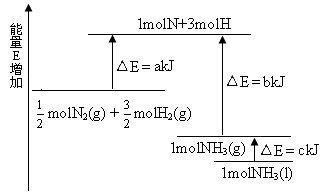
| A.N2(g)+3H2(g) ="==" 2NH3(1)△H=2(a-b-c)kJ·mol-1 |
| B.N2(g)+3H2(g) ="==" 2NH3(g)△H=2(b-a)kJ·mol-1 |
C.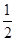 N2(g)+ N2(g)+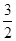 H2(g) ===NH3(1)△H=(b+c-a)kJ·mol-1 H2(g) ===NH3(1)△H=(b+c-a)kJ·mol-1 |
D.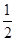 N2(g)+ N2(g)+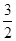 H2(g) ===NH3(g)△H=(a+b)kJ·mol-1 H2(g) ===NH3(g)△H=(a+b)kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a > b | B.a = b | C.a < b | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.565kJ | B.282.5kJ | C.765kJ | D.380kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应为放热反应 |
| B.反应物的总能量大于生成物的总能量 |
| C.该反应中每有4molNH3被氧化,放出1025kJ热量 |
| D.该反应每形成6molH—O键,放出1025kJ热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.-44.2 kJ·mol-1 | B.+44.2 kJ·mol-1 编号 起始状态(mol) 平衡时HBr(g) 物质的量(mol) |
| C.-330 kJ·mol-1 | D.+330 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2 L液态水分解成2L氢气与1L氧气吸收571.6kJ热量 |
| B.2 mol氢气与1mol氧气反应生成2mol气态水放出热量大于571.6kJ |
| C.在相同条件下,2 mol氢气与1mol氧气的能量总和大于2mol液态水的能量 |
| D.使用催化剂能降低该反应的活化能使反应放出得热量小于571.6kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com