
| A�� | �ɷ�Ӧ��ȷ��������������O2 | |
| B�� | ������ֽ����û������lmol�����������Ϊ45g����Ӧ����ʽ�ɱ�ʾΪ��3HClO3�T2O2��+C12��+HClO4+H2O | |
| C�� | �ɷǽ�����Cl��S������֪����HClO3��H2SO4 | |
| D�� | ����ѧ������a=8��b=3����÷�Ӧת�Ƶ�����Ϊ8e- |
���� A������HClO3�������������ǻ�ԭ����HClO4��O2���������
B������������ʵ���������ȷ��b��c���ٽ��������ԭ��Ӧ����ѭԭ�ӡ������غ������
C���ɷǽ�����Cl��S������������Ӧˮ���������Խǿ��
D���ӻ��ϼ۱仯�ĽǶȼ���ת�Ƶĵ�������
��� �⣺A������HClO3�������������ǻ�ԭ����HClO4��O2���������Cl2�ǻ�ԭ�����A����
B����1mol�����������Ϊ45g����n��Cl2��+n��O2��=1mol��n��Cl2����71g/mol+n��O2����32g/mol=45g�����n��Cl2��=$\frac{2}{3}$mol��n��O2��=$\frac{1}{3}$mol����n��Cl2����n��O2��=2��1����b=2c=2�����ɵ����غ��d����7-5��+b��4=c��2����5-0������d����7-5��+2��4=1��2����5-0�������d=1������Clԭ���غ��a=2c+d=3���ٸ���Hԭ���غ���a=d+2e����e=1���ʸ�����·�Ӧ����ʽΪ3HClO3=2O2��+Cl2��+HClO4+H2O����B��ȷ��
C���ɷǽ�����Cl��S������������Ӧˮ���������Խǿ������֪����HClO4��H2SO4����C����
D������ѧ������a=8��b=3����ѧ��Ӧ����ʽΪ8HClO3=3O2��+2 Cl2��+4 HClO4+2H2O����ԭ����ֻ��Cl2����HClO3��Cl2��ClԪ�ػ��ϼ���+5�۽���Ϊ0�ۣ�������2molCl2ʱת�Ƶ��ӵ����ʵ���Ϊ2mol��2����5-0��=20mol�����÷�Ӧ�е���ת����ĿΪ20e-����D����
��ѡB��
���� ���⿼��������ԭ��Ӧ��Ϊ��Ƶ���㣬���շ�Ӧ��Ԫ�صĻ��ϼ�Ϊ�����Ĺؼ���ע�ⷴӦ���غ㷨Ӧ�ü�����ת�Ƽ��㷽������Ŀ�ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH��Һ | B�� | Ba��OH��2��Һ | C�� | ��ˮ | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
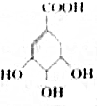 �Ǵ�������ϡ��˽ǡ���ȡ��һ���л���Ǻϳɿ�������ҩ��Ļ���ԭ�ϣ�1molç������������Na��NaOH��Ӧ�����ĵ�Na��NaOH�����ʵ���֮��Ϊ��������
�Ǵ�������ϡ��˽ǡ���ȡ��һ���л���Ǻϳɿ�������ҩ��Ļ���ԭ�ϣ�1molç������������Na��NaOH��Ӧ�����ĵ�Na��NaOH�����ʵ���֮��Ϊ��������| A�� | 4��1 | B�� | 1��1 | C�� | 3��1 | D�� | 1��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 80% | B�� | 60% | C�� | 40% | D�� | 33.3% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ��ʯ����ȼú�������� | |
| B�� | ������������Ư���̲�Ʒ���� | |
| C�� | ̼��������θ����� | |
| D�� | ��FeCl2��Һ��ͭ��Ӧ����ӡˢ��·�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �÷�Ӧ�е���������SiO2����ԭ��ΪC | |
| B�� | �÷�Ӧ�е��������ͻ�ԭ�������ʵ���֮��Ϊ1��3 | |
| C�� | �÷�Ӧ��ÿ����1 mol SiCת��4 mol���� | |
| D�� | �÷�Ӧ�еĻ�ԭ������SiC������������CO�������ʵ���֮��Ϊ1��2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com