
| A. | (CH3)3COH的名称:1,1-二甲基乙醇 | B. | 有机物CH3CH=CHCH2OH的键线式为: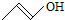 | ||
| C. | 乙醇分子的球棍模型: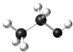 | D. | 氨基的电子式: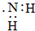 |
分析 A.该有机物分子中,羟基位于2号C,主链为丙醇;
B.键线式中应该用用短线表示出O-H键;
C.球棍模型中用短线和大小不同小球表示有机物组成和结构;
D.氨基中N原子最外层电子数为7.
解答 解:A.(CH3)3COH中主链含有3个C,羟基在2号C,正确名称是:2-甲基-2-丙醇,故A错误;
B.有机物CH3CH=CHCH2OH的键线式中应该用短线表示出O-H键,正确的键线式为: ,故B错误;
,故B错误;
C.乙醇分子中含有1个甲基、1个亚甲基和1个羟基,其球棍模型为: ,故C正确;
,故C正确;
D.氨基中氮原子最外层为7个电子,含有3个氮氢共用电子对,氨基正确的电子式为: ,故D错误;
,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、键线式、有机物命名、球棍模型等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ①②④ | C. | ②④⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al 和Mg | B. | K和 Na | C. | Na 和Al | D. | Zn 和Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
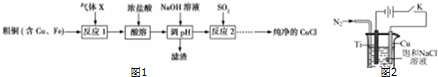
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4molA+2molB | B. | 3molC+1molD+2molA+1molB | ||
| C. | 3molC+1molD+1molB | D. | 3molC+1molD |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com