
普通泡沫灭火器的铁筒里装着一只小玻璃筒,玻璃筒内盛装硫酸铝溶液,铁筒里盛装碳酸氢钠饱和溶液。使用时,倒置灭水器,两种药液相混合就会喷出含二氧化碳的白色泡沫。
(1)产生此现象的化学方程式是
________________________________________________________________________
________________________________________________________________________。
不能把硫酸铝溶液装在铁筒里的主要原因是
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
一般不用碳酸钠代替碳酸氢钠,是因为
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(1)Al2(SO4)3+6NaHCO3===3Na2SO4+2Al(OH)3↓+6CO2↑ (2)因Al3+发生水解:Al3++3H2O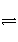
 Al(OH)3+3H+,溶液呈酸性会腐蚀铁筒 (3)与等物质的量的Al2(SO4)3反应Na2CO3产生CO2的量较少,且生成CO2的速率慢
Al(OH)3+3H+,溶液呈酸性会腐蚀铁筒 (3)与等物质的量的Al2(SO4)3反应Na2CO3产生CO2的量较少,且生成CO2的速率慢
解析 硫酸铝溶液和碳酸氢钠溶液相遇会发生双水解反应产生CO2气体和氢氧化铝泡沫达到灭火的目的,其原理是:Al2(SO4)3+6NaHCO3===3Na2SO4+2Al(OH)3↓+6CO2↑。若把硫酸铝溶液放在铁筒中,因Al3+发生水解:Al3++3H2O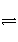
 Al(OH)3+3H+,溶液呈酸性会腐蚀铁筒。如果用Na2CO3代替NaHCO3,则发生的双水解反应是:Al2(SO4)3+3Na2CO3+3H2O===3Na2SO4+2Al(OH)3↓+3CO2↑,可见,与等物质的量的Al2(SO4)3反应时Na2CO3产生CO2的量较少,且生成CO2的速率慢。
Al(OH)3+3H+,溶液呈酸性会腐蚀铁筒。如果用Na2CO3代替NaHCO3,则发生的双水解反应是:Al2(SO4)3+3Na2CO3+3H2O===3Na2SO4+2Al(OH)3↓+3CO2↑,可见,与等物质的量的Al2(SO4)3反应时Na2CO3产生CO2的量较少,且生成CO2的速率慢。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
在下列平衡2CrO42-(黄色)+ 2H+ Cr2O72-(橙红色)+ H2O中,溶液介于黄和
Cr2O72-(橙红色)+ H2O中,溶液介于黄和
橙红色之间,今欲增加溶液的橙红色,则要在溶液中加入
A.H+ B.OH- C.K+ D.H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
目前流行的关于生命起源假设的理论认为,生命起源于约40亿年前的古洋底的热液环境,这种环境系统中普遍存在铁硫簇结构,如Fe2S2、Fe4S4、Fe8S7等,这些铁硫簇结构参与了生命起源的相关反应。某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验。
【实验Ⅰ】 确定硫的质量:
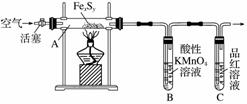
按图连接装置,检查好装置的气密性后,在硬质玻璃管A中放入1.0 g铁硫簇结构(含有部分不反应的杂质),在试管 B中加入50 mL 0.100 mol·L-1的酸性KMnO4溶液,在试管C中加入品红溶液。通入空气并加热,发现固体逐渐转变为红棕色。待固体完全转化后,将B中溶液转移至 250 mL 容量瓶,洗涤试管B后定容。取25.00 mL该溶液用0.01 mol·L-1的草酸(H2C2O4)溶液滴定剩余的 KMnO4。记录数据如下:
| 滴定次数 | 待测溶液体积/mL | 草酸溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.50 | 23.70 |
| 2 | 25.00 | 1.02 | 26.03 |
| 3 | 25.00 | 0.00 | 24.99 |
相关反应:①2MnO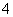 +2H2O+5SO2===2Mn2++5SO
+2H2O+5SO2===2Mn2++5SO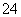 +4H+
+4H+
②2MnO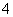 +6H++5H2C2O4===2Mn2++10CO2↑+8H2O
+6H++5H2C2O4===2Mn2++10CO2↑+8H2O
【实验Ⅱ】 确定铁的质量:
将实验Ⅰ硬质玻璃管A中的残留固体加入稀盐酸中,充分搅拌后过滤,在滤液中加入足量的NaOH溶液,过滤后取滤渣,经充分灼烧得0.6 g固体。
试回答下列问题:
(1)判断滴定终点的方法是____________________。
(2)试管C中品红溶液的作用是__________________________________________。
有同学提出,撤去C装置对实验没有影响,你的看法是________(选填“同意”或“不同意”),理由是____________________________。
(3)根据实验Ⅰ和实验Ⅱ中的数据可确定该铁硫簇结构的化学式为____________________。
【问题探究】 滴定过程中,细心的同学发现该KMnO4溶液颜色褪去的速率较平常滴定时要快得多。为研究速率加快的原因,该同学继续进行了下列实验,实验数据如下表:
| 编号 | 温度/℃ | 酸化的H2C2O4溶液/mL | KMnO4溶液/mL | 溶液褪色时间/s |
| 1 | 25 | 5.0 | 2.0 | 40 |
| 2 | 25 | 5.0(另加少量可溶于水的MnSO4粉末) | 2.0 | 4 |
| 3 | 60 | 5.0 | 2.0 | 25 |
(4)分析上述数据,滴定过程中反应速率加快的一种可能原因是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关n、l、m、ms四个量子数的说法中,不正确的是( )
A.一般而言,n越大,电子离核的平均距离越远,能量越高
B.l的数值多少,决定了某电子层不同能级的个数
C.对于确定的n值,m的取值共有2n+1个
D.ms可用“↑”和“↓”标记,不同符号表示电子的自旋方向不同
查看答案和解析>>
科目:高中化学 来源: 题型:
为了同时对某农作物施用分别含有N、P、K三种元素的化肥,对于给定的化肥中,最适合的组合是( )
①K2CO3 ②KCl ③Ca(H2PO4)2 ④(NH4)2SO4 ⑤氨水
A.①③④ B.②③④ C.①③⑤ D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的值。下列说法正确的是( )
A.一定条件下,0.2 mol SO2与足量O2充分反应,生成SO3分子数为0.2NA
B.0.1 mol —NH2(氨基)中含有的电子数为0.7NA
C.3.4 g H2O2中含有的共用电子对数为0.1NA
D.常温常压下,16 g O2和O3混合气体含有的氧原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会( )
A.偏大 B.偏小 C.无影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com