
“生物质”是指由植物或动物生命体衍生得到的物质的总称。 “生物质能”主要指用树木、庄稼、草类等植物直接或间接提供的能量。下面有关“生物质能”的说法,不正确的是 ( )
A.利用生物质能就是间接利用太阳能 B.生物质能源是可再生的能源
C.生物质能源是解决农村能源的主要途径 D.生物质能的缺点是严重污染环境
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:填空题
(1)判断下列说法,正确的是 。
①某有机物完全燃烧后生成二氧化碳和水,说明该有机物中必定含有C、H、O3种元素
②煤的干馏是化学变化,石油分馏也是化学变化,煤的气化是物理变化
③淀粉、纤维素、油脂、蛋白质可以作为营养物质被人利用和吸收
④将蔗糖放入试管中,加水和稀硫酸震荡,水溶加热5分钟,取水3ml加入新制的Cu(OH)2,加热后没有看到砖红色物质出现,这是因为加热时间不够;
⑤油脂在碱性条件下水解反应成为皂化反应
⑥聚乙烯、聚氯乙烯、聚苯乙烯等高分子化合物都是由加聚反应制得的
⑦海水淡化的主要方法是蒸馏法、电渗析法、离子交换法等。其中蒸馏法历史最久,技术和工艺成熟且成本低。
(2)碳原子数四到十的烷烃中其一氯化物只有一种的是 (写结构简式)
(3)苯环上发生溴化所用的试剂和条件 ,该反应的反应类型为 。
(4)两气体a、b分别为0.6mol与0.5mol。在0.4L密闭容器中发生反应2a+b mc+d,经5min后达到平衡,此时c为0.2mol.又知在此反应期间d的平均反应速率为0.1mol·L-1·min-1,求
mc+d,经5min后达到平衡,此时c为0.2mol.又知在此反应期间d的平均反应速率为0.1mol·L-1·min-1,求
①m的值为 ②b的转化率为 ③a的平均反应速率为 ④写出计算过程 ;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期中化学试卷(解析版) 题型:选择题
下列有关化学反应速率的说法正确的是
A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
B.100mL2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C.SO2的催化氧化时一个放热的反应,所以升高温度,反应速率减慢
D.汽车尾气中的NO和CO可以缓慢生成N2和CO2,减小压强,反应速率减慢
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:填空题
如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中。试回答下列问题:
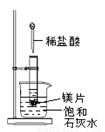
(1)实验中观察到的现象是____________________;
(2)产生上述现象的原因是____________________;
(3)写出有关的离子方程式:________________ __。
(4)由实验推知,反应中生成MgCl2和H2形成化学键时
所释放的总能量____(填“大于”“小于”或“等于”)消耗镁片和盐酸时断裂化学键所吸收的总能量。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
形成原电池的条件一般有:①电解质溶液;②两个电极;③能自发地发生氧化还原反应;④形成闭合回路,请根据上述条件判断下列装置中属于原电池的是( )
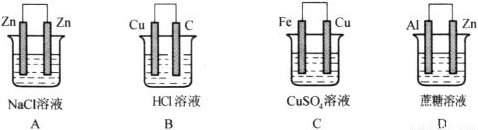
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
下列有关氢化物的叙述中正确的( )
A.气态氢化物稳定性:PH3 > CH4
B.HCl的电子式为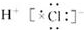
C.D2O分子所有原子均达到最外层8e—稳定结构
D.VIIA族元素中F的最高价氧化物对应水化物酸性最强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
雷雨天闪电时空气中有臭氧生成,下列说法正确的是( )
A.16O2和18O3互为同位素
B.O2和O3的相互转化是物理变化
C.等物质的量的O2和O3含有相同的质子数
D.等质量的O2和O3含有相同的O原子数
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三第六次适应性考试理综化学试卷(解析版) 题型:填空题
二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
编号 | 热化学方程式 | 化学平衡常数 |
① | CO(g)+2H2(g) | K1 |
② | 2CH3OH(g) | K2 |
③ | CO(g)+H2O(g) | K3 |
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
化学键 | H-H |
| C=O | H-O | C-H |
E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
由上述数据计算ΔH1= 。
(2)该工艺的总反应为3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) ΔH
CH3OCH3(g)+CO2(g) ΔH
该反应ΔH= ,化学平衡常数K= (用含K1、K2、K3的代数式表示)。
(3)下列措施中,能提高CH3OCH3产率的有________。
A.分离出二甲醚 B.升高温度
C.改用高效催化剂 D.增大压强
(4)工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生。该工艺中反应③的发生提高了CH3OCH3的产率,原因是_______________________________。
(5)以=2 通入1 L的反应器中,一定条件下发生反应:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) ΔH,其CO的平衡转化率随温度、压强变化关系如图所示。下列说法正确的是____。
CH3OCH3(g)+H2O(g) ΔH,其CO的平衡转化率随温度、压强变化关系如图所示。下列说法正确的是____。
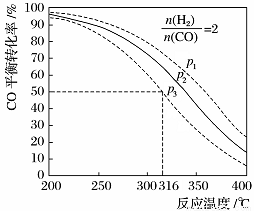
A.该反应的ΔH>0
B.若在p2和316℃时反应达到平衡,则CO的转化率小于50%
C.若在p3和316℃时反应达到平衡,H2的转化率等于50%
D.若在p3和316℃时,起始时=3,则达平衡时CO的转化率大于50%
E.若在p1和200℃时,反应达平衡后保持温度和压强不变,再充入2 mol H2和1 mol CO,则平衡时二甲醚的体积分数增大
(6)某温度下,将8.0mol H2和4.0mol CO充入容积为2 L的密闭容器中,发生反应:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g),反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数K= 。
CH3OCH3(g)+H2O(g),反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数K= 。
查看答案和解析>>
科目:高中化学 来源:2016届江西南昌二中、临川一中等高三4月联考二理综化学试卷(解析版) 题型:填空题
发展洁净煤技术、利用CO2制备清洁能源等都是实现减碳排放的重要途径。
(1)将煤转化成水煤气的反应:C(s)+H2O(g)  CO(g)+H2(g)可有效提高能源利用率, 若在上述反应体系中加入催化剂(其他条件保持不变),此反应的△H ________(填“增大”、“减小”或“不变”)。
CO(g)+H2(g)可有效提高能源利用率, 若在上述反应体系中加入催化剂(其他条件保持不变),此反应的△H ________(填“增大”、“减小”或“不变”)。
(2)CO2制备甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g); ΔH=-49.0 kJ·mol-1,
CH3OH(g)+H2O(g); ΔH=-49.0 kJ·mol-1,
在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2(g) 和CH3OH(g)
浓度随时间变化如图1所示

①0~9min时间内,该反应的平均反应速率ν(H2) = _________________________。
②在相同条件下,密闭容器的体积压缩至0.5 L时,此反应达平衡时放出的热量(Q)可能是________(填字母序号)kJ。
a. 0 < Q < 29.5 b. 29.5 < Q < 36.75 c. 36.75 < Q < 49 d. 49 < Q < 98
③在一定条件下,体系中CO2的平衡转化率(α)与L和X的关系如图2所示,L和X 分别表示温度或压强。
i. X表示的物理量是 ________________ 。
ii. 判断L1与L2的大小关系,并简述理由:________。
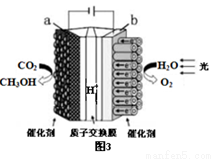
(3)利用铜基催化剂光照条件下由CO2和H2O制备CH3OH的装置示意图如图3所示,该装置工作时阴极的电极反应式是_____________________。
(4)利用CO2和NH3为原料也合成尿素,在合成塔中的主要反应可表示如下:
反应①:2NH3(g)+CO2(g) 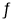 NH2CO2NH4(s) △H1= __________________。
NH2CO2NH4(s) △H1= __________________。
反应②:NH2CO2NH4(s) 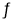 CO(NH2)2(s)+H2O(g) △H2=+72.49kJ·mol-1
CO(NH2)2(s)+H2O(g) △H2=+72.49kJ·mol-1
总反应:2NH3(g)+CO2(g) 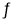 CO(NH2)2(s)+H2O(g) △H=-86.98kJ·mol-1;
CO(NH2)2(s)+H2O(g) △H=-86.98kJ·mol-1;
则反应①的△H1=_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com