
| A. | 高炉炼铁、生产普通硅酸盐水泥和普通玻璃都要用到的原料是石灰石 | |
| B. | 用电解饱和食盐水的方法制备金属钠 | |
| C. | 通常用海水提取食盐后的母液为原料制取溴单质 | |
| D. | 利用焦炭在高温下还原二氧化硅可制备粗硅 |
分析 A.高炉炼铁的原料:铁矿石、焦炭、石灰石;制硅酸盐水泥的原料:石灰石和黏土;制普通玻璃的原料:石英砂、石灰石、纯碱等;
B.饱和氯化钠溶液在通电的条件下生成氢氧化钠、氢气和氯气,用电解食盐固体的方法制备金属钠;
C.溴元素的99%存在于海洋,称作“海洋元素”,提取食盐后的盐水母液为原料可制取溴单质;
D.焦炭高温还原二氧化硅生成一氧化碳和硅.
解答 解:A.高炉炼铁的原料:铁矿石、焦炭、石灰石;生产普通硅酸盐水泥的原料:石灰石和黏土;制普通玻璃的原料:石英砂、石灰石、纯碱,所以高炉炼铁、生产普通硅酸盐水泥和普通玻璃都要用到的原料是石灰石,故A正确;
B.饱和氯化钠溶液在通电的条件下生成氢氧化钠、氢气和氯气,化学方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,用电解食盐固体的方法制备金属钠,反应为:2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑,故B错误;
C.海水中的溴元素以溴离子的形式存在,通常用海水提取食盐后的母液为原料制取溴单质,氯气可以将溴离子氧化为溴单质,即2Br-+C12=Br2+2Cl-,将生成的溴单质从其水溶液中分离出来,可以采用萃取法,向其中加入四氯化碳,在震荡,下层的即为溶有溴单质的四氯化碳混合物,然后再采用蒸馏的方法实现溴单质和四氯化碳的分离,故C正确;
D.焦炭高温还原二氧化硅生成一氧化碳和硅,化学方程式:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,可制备粗硅,故D正确;
故选B.
点评 本题主要考查了工业生产的原理、原料,题目难度不大,注意基础知识的掌握和原理的灵活应用.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:选择题
| A. | 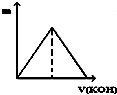 | B. | 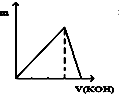 | C. | 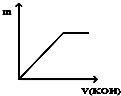 | D. | 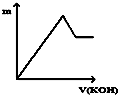 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用装置氧化废液中的溴化氢 | B. | 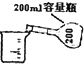 量取100.00mL溶液 | ||
| C. | 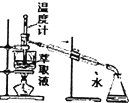 将萃取液中的苯与碘进行分离 | D. |  灼烧熔融碳酸钠固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠保存在细口瓶中并加煤油液封 | |
| B. | 新制氯水保存在棕色瓶中并置于冷暗处 | |
| C. | NaOH溶液保存在无色试剂瓶中并要塞紧橡胶塞 | |
| D. | 硫酸亚铁溶液存放在加有少量铁粉的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、K+、SO42-、HCO3- | B. | Mg2+、Na+、SO42-、Cl- | ||
| C. | Na+、K+、SO42-、NO3- | D. | Ba2+、Na+、MnO4-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{2}$(10-9+10-11) mol•L-1 | B. | 2×10-11mol•L-1 | ||
| C. | (1×10-14-5×10-4) mol•L-1 | D. | (10-9+10-11) mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com