
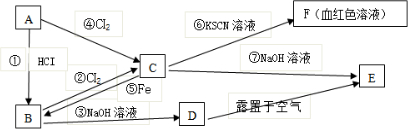
分析 A是常见的金属,C的溶液呈现黄色,且C与KSCN溶液混合溶液为血红色,则C含有Fe3+,由元素守恒可知,A为Fe,结合转化关系可知,C为FeCl3,B为FeCl2,D为Fe(OH)2,E为Fe(OH)3,F为Fe(SCN)3,结合对应物质的性质以及题目要求解答该题.
解答 解:(1)由以上分析可知A为Fe,故答案为:Fe;
(2)C为FeCl3,与氢氧化钠溶液反应生成氢氧化铁,为红褐色沉淀,故答案为:产生红褐色沉淀;
(3)铁为活泼金属,与盐酸发生置换反应生成氢气,故答案为:置换;
(4)铁离子可与KSCN发生显色反应,溶液变为血红色,亚铁离子具有还原性,可与高锰酸钾等溶液发生氧化还原反应而使高锰酸钾的紫色消失,可取少量待测液,滴加KSCN溶液,溶液变血红色,说有待测液中有Fe3+;取少量待测液,滴加高锰酸钾酸性溶液,紫色消失,说有待测液中有Fe2+,故答案为:取少量待测液,滴加KSCN溶液,溶液变血红色,说有待测液中有Fe3+;取少量待测液,滴加高锰酸钾酸性溶液,紫色消失,说有待测液中有Fe2+;
(5)氢氧化亚铁不稳定,在空气中被氧化生成氢氧化铁,方程式为4Fe(OH)2+O2+2H2O=4 Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O=4 Fe(OH)3.
点评 本题考查无机物的推断,为高频考点,侧重考查学生的分析能力,注意C与KSC溶液呈血红色是推断的突破口,明确铁离子的颜色及检验方法是解答本题的关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若温度不变,容器体积缩小到原来的一半,此时A的浓度是原来的1.75倍,则a+b<c+d | |
| B. | 若温度不变,容器体积缩小到原来的一半,A的转化率可能不增大 | |
| C. | 若a+b=c+d,则对于体积不变的容器,升高温度平衡向左移动,容器中气体的压强不变 | |
| D. | 混合气体的平均相对分子质量不再变化是该反应达到平衡的标志之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
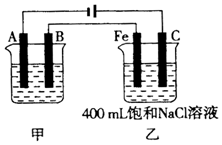 如图为相互串联的甲、乙两电解池.
如图为相互串联的甲、乙两电解池.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 g氢气所含原子数为NA | |
| B. | 常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA | |
| C. | 在常温常压下,11.2LN2所含原子数为NA | |
| D. | 2.7g金属铝和足量盐酸反应,失去的电子数目为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com