

| A. | 该过程中产生标准状况下4.48L H2 | |
| B. | 向c点处的反应液中加入稀盐酸后无明显现象 | |
| C. | 图中a=1.5 | |
| D. | 当加入铁粉n mol时(0.1<n<0.15),溶液中n(Fe3+)=(0.3-2n)mol |
分析 A、产生的气体是一氧化氮;
B、加入稀盐酸,氢离子、硝酸根离子和亚铁离子发生氧化还原反应;
C、成的气体只有一种,生成HNO3的还原产生是一氧化氮,氧化性硝酸占整个硝酸的$\frac{1}{4}$;
D、硝酸与铁反应生成铁离子时最大量消耗铁的物质的量为:0.2L×2mol•L-1=0.4mol,所以氧化的硝酸的物质的量为:0.4mol×$\frac{1}{4}$=0.1mol,所以转移电子的物质的量为0.3mol,所以参加反应铁的最大量为:0.1mol.
解答 解:A、产生的气体是一氧化氮,而不是氢气,故A错误;
B、加入稀盐酸,氢离子、硝酸根离子和亚铁离子发生氧化还原反应,所以现象是有气泡产生,气体遇空气变红棕色,故B错误;
C、成的气体只有一种,生成HNO3的还原产生是一氧化氮,氧化性硝酸占整个硝酸的$\frac{1}{4}$,所以氧化的硝酸的物质的量为:0.4mol×$\frac{1}{4}$=0.1mol,根据转移电子的物质的量相等,所以亚铁离子的物质的量为:$\frac{0.1×3}{2}$=0.15mol,所以a=0.15,故C错误;
D、硝酸与铁反应生成铁离子时最大量消耗铁的物质的量为:0.2L×2mol•L-1=0.4mol,所以氧化的硝酸的物质的量为:0.4mol×$\frac{1}{4}$=0.1mol,所以转移电子的物质的量为0.3mol,所以参加反应铁的最大量为:0.1mol,所以b=0.1mol,则根据电子转移相等,3n(Fe3+)+2n(Fe2+)=0.1×3,所以n(Fe3+)=(0.3-2n)mol,故D正确;
故选D.
点评 本题考查学生金属铁所发生的氧化还原反应知识,注意平时知识的积累是解题的关键,综合性较强,结合图象考查增加了难度.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | 仅①③ | B. | 仅②③ | C. | 仅①② | D. | 仅③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发皿 | B. | 漏斗 | C. | 蒸馏烧瓶 | D. | 容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钙、铁、锌、硒都是人体必需的微量元素 | |
| B. | 发现煤气泄漏应立即关闭阀门,开窗通风 | |
| C. | 用肥皂水可鉴别硬水和软水 | |
| D. | 氢能源的大量应用需解决制取成本高、贮存困难等问题 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )中所含有的共价键数目为( )
)中所含有的共价键数目为( )| A. | NA | B. | 0.7NA | C. | 1.9NA | D. | 7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,AgCl的溶解度减小 | |
| B. | 在任何含AgCl固体的水溶液中,c(Ag+)=c(Cl-)且二者乘积是一个常数 | |
| C. | AgCl沉淀生成和溶解不断进行,但速率相等 | |
| D. | 向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解的质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
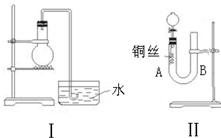 实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果.根据要求回答下列问题:
实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果.根据要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
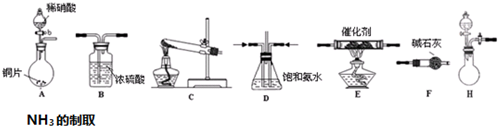
| 试剂组合序号 | 固体试剂(g) | NH3体积(mL) | |
| a | 12.0g Ca(OH)2 (过量) | 10.8g NH4Cl | 2688 |
| b | 10.8g (NH4)2SO4 | 2728 | |
| c | 12.0g NaOH (过量) | 10.8g NH4Cl | 3136 |
| d | 10.8g (NH4)2SO4 | 3118 | |
| e | 12.0g CaO (过量) | 10.8g NH4Cl | 3506 |
| f | 10.8g (NH4)2SO4 | 3584 | |
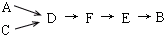
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com