
下列说法中正确的是( )
A、煤燃烧是化学能转化为光能的过程
B、1 mol 甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
C、HCl 和 NaOH 反应的中和热 ΔH=-57.3 kJ·mol-1,则 H2SO4 和 Ca(OH)2 反应中和热
ΔH=2×(-57.3)kJ·mol-1
D、反应 H2(g)+F2(g)===2HF(g);ΔH=-270 kJ·mol-1说明在相同条件下,1 mol 氢气与 1 mol 氟气的能量总和大于2 mol 氟化氢气体的能量
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列依据热化学方程式得出的结论正确的是
A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6KJ·mol-1,则氢气的燃烧热为241.8kJ·mol-1
B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1);△H=-57.4kJ·mol-1则含 20.0gNaOH的稀溶液与稀醋酸完全中和,放出小于28.7kJ的热量
C.已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定
D.己知2C(s)+2O2(g)=2CO2(g);△H=akJ·mol-1、 2C(s)+O2(g)=2CO(g); △H= bkJ·mol-1,则a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
已知3.2g某气体中含有3.01×1022个分子,此气体的摩尔质量是( )
|
| A. | 32 g/mol | B. | 64 | C. | 64 g/mol | D. | 4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
欲用98%的浓硫酸,(密度为1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500ml.
(1)请将下列各操作,按正确的序号填在横线上.
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线
D.洗净所用仪器
E.稀释浓H2SO4F.将溶液转入容量瓶
其操作正确的顺序依次为 D、A、E、D、C、B .
(2)简要回答下列问题:(每空1分,共9分)
①所需浓硫酸的体积为 mL.
②如果实验室有15mL、20mL、50mL的量筒应选用 mL的量筒最好,量取时发现量筒不干净用水洗净后直接量取将使浓度 (“偏高”、“偏低”、“无影响”以下同)
③将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并用玻璃棒不断搅拌,若搅拌过程中有液体溅出,结果会使所配溶液浓度 .
④在转入容量瓶前烧杯中液体应 静置冷却 ,否则会使浓度 ;并洗涤烧杯和玻璃棒2~3次,洗涤液也要转入容量瓶,否则会使浓度 .
⑤定容时必须使溶液凹液面与刻度线相切,若俯视会使浓度 ;仰视则使浓度 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下在容积为 2L 的密闭容器中,发生反应 2X(g) + Y(g) 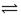 2W(g);△H<0,当充入 2 mol X 和 1 mol Y,经20 s达到平衡时生成了 0.4 molW。下列说法正确的是()
2W(g);△H<0,当充入 2 mol X 和 1 mol Y,经20 s达到平衡时生成了 0.4 molW。下列说法正确的是()
①升高温度,W 的体积分数减小,△H 增大
②以 Y 的浓度变化表示的反应速率为 0.01 mol/(L·s)
③在其它条件不变的情况下,增加 1 mol X ,则 X 和 Y 的转化率均提高
④增大压强,正反应速率增大,逆反应速率减小,则平衡向正反应方向移动
⑤再向容器中通入 2 mol X 和 1 mol Y,达到平衡时,X 、Y 的转化率均增大。
、Y 的转化率均增大。
A、①⑤ B、⑤ C、②③④ D、④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
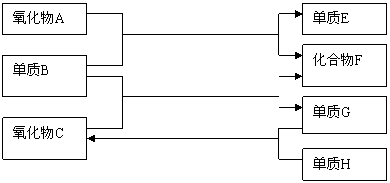
已知CO和H2的混合气体称为水煤气,可由碳与水蒸气在高温下反应生成。如下图:
高温
反应①

 高温
高温
反应②
燃烧
反应③
已知:单质E可作为半导体材料,化合物F是有毒的氧化物,C为液态。据此,请填空:
(1)氧化物A是
(2)化合物F是
(3)反应②的化学方程式是
(4)反应③的化学方程式是
查看答案和解析>>
科目:高中化学 来源: 题型:
有关杂化轨道的说法不正确的是
A.杂化前后的轨道数不变,但轨道的形状发生了改变
B.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180°
C.四面体形、三角锥形、V形分子的结构可以用sp3杂化轨道解释
D.杂化轨道全部参加形成化学键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com