
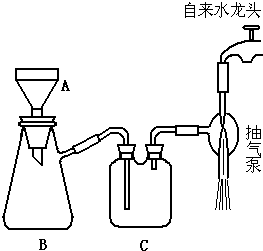
分析 减压过滤装置一般用到布氏漏斗、吸滤瓶以及安全瓶等,操作时注意防止固体堵住吸滤瓶以及倒吸等现象,以此解答该题.
解答 解:(1)由题给装置可知A为布氏漏斗,B为吸滤瓶,C为安全瓶,故答案为:布氏漏斗;吸滤瓶;安全瓶;
(2)该装置图有三处错误:分别是①布氏漏斗插入过深,不应超过$\frac{2}{3}$;②了让收率效率更高.斜面朝向支管口,则漏斗斜面口部的空气很快被优先抽走,形成负压.滤液会更快的被抽滤下来;
③安全瓶导管左长右短,应左短右长,防止倒吸.
故答案为:布氏漏斗插入过深,不应超过$\frac{2}{3}$;布氏漏斗下端斜口未对支管口,应对支管口;安全瓶导管左长右短,应左短右长.
点评 本题考查物质的分离、提纯,侧重于学生的分析能力和实验能力的考查,题目涉及减压分离,注意把握实验的原理以及所用仪器的使用方法,难度不大.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案科目:高中化学 来源: 题型:实验题
 乙二酸俗称草酸是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示)填空:
乙二酸俗称草酸是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示)填空:| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、K+、SO42-、Cl-、Al[(OH)4]- | B. | Al3+、Na+、Cl-、SO42-、NO3- | ||
| C. | Na+、K+、SO42-、NO3-、Cl- | D. | Fe2+、H+、Br-、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色气体,难溶于水,密度比空气略小 | |
| B. | 乙烯燃烧时,火焰明亮,同时产生黑烟 | |
| C. | 与溴水发生取代反应而使溴水褪色 | |
| D. | 乙烯的产量标志着一个国家的石油化工水平 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子晶体中只含有离子键,不含有共价键 | |
| B. | 水分子很稳定,因为水分子间存在氢键 | |
| C. | 分子晶体中一定存在分子间作用力,不一定存在共价键 | |
| D. | I的原子半径大于Br,HI比HBr的热稳定性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
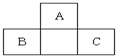 A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C两元素在周期表中族序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )
A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C两元素在周期表中族序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )| A. | Be、Na、Al | B. | B、Mg、Si | C. | C、Al、P | D. | O、P、Cl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com