
【题目】以苯和乙炔为原料合成化工原料H的路线如下:
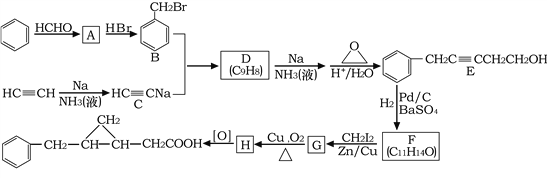
回答下列问题:
(1)A的名称____________,E中的官能团名称为_____________________________。
(2)苯和甲醛反应生成A的反应类型为___________,B和C反应生成D的反应类型为___________。
(3)F的结构简式为_________,G生成H的化学方程式为_____________________________。
(4)B的亚甲基(—CH2—)的一个H被Br再取代生成I(![]() ),含有苯环的I的同分异构体共有__________种(不含I),其中核磁共振氢谱有三组峰,且峰面积之比为1:1:1的结构简式为_____________。
),含有苯环的I的同分异构体共有__________种(不含I),其中核磁共振氢谱有三组峰,且峰面积之比为1:1:1的结构简式为_____________。
(5)参照上述合成路线,设计一条以乙炔和必要试剂合成环丙烷的路线。写出合成路线:
________________________________________________________________________。
【答案】 苯甲醇 碳碳三键、羟基 加成反应 取代反应 ![]()
 9
9 ![]()
![]()
【解析】苯与甲醛发生加成反应生成A为![]() ,A与HBr发生取代反应生成
,A与HBr发生取代反应生成![]() ,
,![]() 与HC≡CNa发生取代反应生成D为
与HC≡CNa发生取代反应生成D为![]() .
.![]() 与氢气发生加成反应生成F,结合F的分子式可知F为
与氢气发生加成反应生成F,结合F的分子式可知F为![]() ,结合
,结合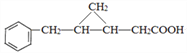 的结构可知F与CH2I2反应生成G为
的结构可知F与CH2I2反应生成G为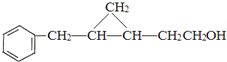 ,G催化氧化生成H为
,G催化氧化生成H为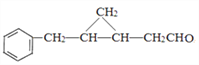 ,最后再氧化得
,最后再氧化得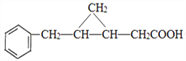 ;
;
(1)![]() 的名称苯甲醇,
的名称苯甲醇,![]() 中的官能团名称为碳碳三键、羟基 ;
中的官能团名称为碳碳三键、羟基 ;
(2)苯和甲醛反应生成![]() 的反应类型为加成反应,
的反应类型为加成反应, 和
和![]() 反应生成
反应生成![]() 的反应类型为取代反应;
的反应类型为取代反应;
(3)F的结构简式为![]() ,
, 发生催化氧化生成H的化学方程式为
发生催化氧化生成H的化学方程式为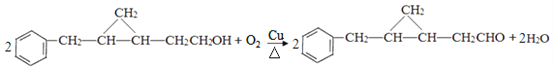 ;
;
(4)![]() 的同分异构体可能是①苯环上有—Br和—CH2B,有邻、间、对共三种;②苯环上有2个—Br和—CH3,其中卤素原子为对位,甲基的位置只有一种;卤素原子为间位,甲基的位置只有三种;卤素原子为邻位,甲基的位置只有二种;则I共有9种同分异构体,其中核磁共振氢谱有三组峰,且峰面积之比为1:1:1的结构简式为
的同分异构体可能是①苯环上有—Br和—CH2B,有邻、间、对共三种;②苯环上有2个—Br和—CH3,其中卤素原子为对位,甲基的位置只有一种;卤素原子为间位,甲基的位置只有三种;卤素原子为邻位,甲基的位置只有二种;则I共有9种同分异构体,其中核磁共振氢谱有三组峰,且峰面积之比为1:1:1的结构简式为![]() ;
;
(5)以乙炔和必要试剂合成环丙烷的路线:![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关于苯的说法中,正确的是( )
A. 苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B. 从苯的凯库勒式( )看,苯分子中含有碳碳双键,应属于烯烃
)看,苯分子中含有碳碳双键,应属于烯烃
C. 在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D. 苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纯净的CaCO3与100 mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积),下列分析正确的是( )

A. OE段表示的平均速率最快
B. EF段,用盐酸表示该反应的平均反应速率为0.4 mol·L-1·min-1
C. OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2∶6∶7
D. F点收集到的CO2的量最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的结构简式如图,下列说法正确的是

A. X分子式为C10H20O,它是环己醇的同系物
B. X分子环上的一氯取代物只有三种
C. X分子中至少有12个原子在同一平面上
D. 在一定条件下,X能发生取代反应、氧化反应、聚合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是( )
A. 洗净的容量瓶可以放进烘箱中烘干
B. 用磨口玻璃瓶保存NaOH溶液
C. 用苯萃取溴水中的溴时,溴的苯溶液从分液漏斗的下口放出
D. 用二硫化碳清洗残留在试管壁上少量的硫粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是
A. H2O2具有强氧化性,可用作消毒剂
B. Fe2(SO4)3易溶于水,可用作净水剂
C. NH3具有还原性可用作制冷剂
D. C2H4具有可燃性可用作催熟剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是

A.X是电源的负极
B.阴极的反应式是:H2O+2e-=H2+O2-,CO2+2e-=CO+O2-
C.总反应可表示为:H2O+CO2![]() H2+CO+O2
H2+CO+O2
D.阴、阳两极生成的气体的物质的量之比是1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是重要的化工原料,用途广泛。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+ 和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是____________。
②醋酸二氨合铜所含元素的单质,所属的晶体类型有________(填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态Cu原子未成对电子数目相同的元素有____种(不含Cu)。
④铜单质为面心立方晶体,其晶胞边长a nm。列式表示铜单质的密度_____ g·cm-3。
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3+NH3=F3B—NH3。
①晶体F3B—NH3中,B原子的杂化轨道类型为 ______________。
②写出两种与BF3具有相同空间构型的阴离子_____________。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。
①下列相关说法中,正确的是_____________(填序号)。
a.N4是N2的同分异构体
b.1 mol N4分解生成N2,形成了4 molπ键
c.白磷的沸点比N4高,是因为P—P键键能比N—N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液与100 mL 0.5 mol·L-1 NaCl溶液中所含Cl-的物质的量浓度相同的是( )
A. 100 mL0.5molL-1 MgCl2溶液 B. 200 mL0.25molL-1 AlCl3溶液
C. 50mL1molL-1 NaCl溶液 D. 25mL 0.5molL-1 HCl溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com