
现有一定量含有Na2O杂质的Na2O2试样,用下图所示的实验装置测定Na2O2试样的纯度。(可供选用的试剂只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
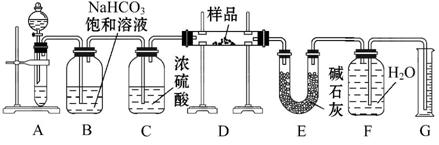
回答下列问题:
(1)装置A中液体试剂选用 ,理由是 ____________________________。
(2)装置B的作用是 _________________________________________________,
装置E中碱石灰的作用是 ____________________________________________。
(3)装置D中发生反应的化学方程式是 ________,_________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为 。
科目:高中化学 来源: 题型:
下列说法正确的是
A.若把H2S分子写成H3S分子,违背了共价键的饱和性
B.H3O+离子的存在,说明共价键不应有饱和性
C.所有共价键都有方向性
D.两个原子轨道发生重叠后,两核间的电子仅存在于两核之间
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.195 g锌粉加入到20.0 mL的0.100 mol·L-1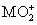 溶液中,恰好完全反应,则还原产物可能是( )
溶液中,恰好完全反应,则还原产物可能是( )
A.M B.M2+ C.M3+ D. MO2+
查看答案和解析>>
科目:高中化学 来源: 题型:
已知2A(g)+B(g)  2C(g),向容积为1 L的密闭容器中加入0.050 mol A和0.025 mol B,在500℃时充分反应,达平衡后测得c(C)=0.040 mol·L-1,放出热量Q1kJ。
2C(g),向容积为1 L的密闭容器中加入0.050 mol A和0.025 mol B,在500℃时充分反应,达平衡后测得c(C)=0.040 mol·L-1,放出热量Q1kJ。
(1)能说明上述反应已经达到化学平衡状态的是 (填写序号);
a.v(C)=2v(B) b.容器内压强保持不变
c.v逆(A)=2v正(B) d.容器内气体的密度保持不变
(2)若在相同的容器中只加入0.050 mol C,500℃时充分反应达平衡后,吸收热量Q2kJ,则Q1与Q2之间的关系式可表示为 (用含Q1、Q2的代数式表示);
(3)500℃时,上述反应的化学平衡常数K= ;
(4)已知:K(300℃)>K(350℃),该反应是 (填“放”或“吸”)热反应;若反应温度升高,A的转化率 (填“增大”“减小”或“不变”);
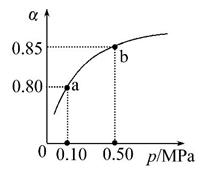
(5)某温度下,A的平衡转化率(α)与体系总压强(p)的关系如图所示,平衡状态由a变到b时,化学平衡常数K(a) K(b)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对于过氧化钠的叙述中,正确的是( )
A.将少量Na2O2投入紫色石蕊试液中,溶液最终呈蓝色
B.1 mol Na2O2与H2O完全反应,转移2 mol电子
C.充分加热等物质的量的Na2O2和NaHCO3的混合物,剩余物质为Na2CO3
D.ag CO和H2的混合气体充分燃烧的产物与足量的Na2O2充分反应后,固体质量增加ag
查看答案和解析>>
科目:高中化学 来源: 题型:
用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选 项 | 操作及现象 | 溶 液 |
| A | 通入CO2,溶液不变浑浊,先通入CO2再通入氨气,溶液变浑浊 | CaCl2溶液 |
| B | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊 | Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来,我国的材料研究迅猛发展,出现了许多具有特殊功能的新型材料。
(1)硅是将太阳能转换为电能的常用材料,从硅的氧化物制取粗硅的化学方程式为______________________________________。
(2)化合物G是开发新一代汽车发动机的新材料。G的相对分子质量为140,含有硅元素,其质量分数为60%,另含有元素Y。E(含两种元素)与NH3反应制得G和HCl。G和E化学式分别为__________________________________ 。
常压条件下向G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,化学通式可表示为Si6-xOxY8-x。在接近1 700℃时x的极限值约为4.0,则化合物中Y元素的化合价为 ____。
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Zn、Ni且均显+2价,下同)由铁酸盐(MFe2O4)经高温被H2还原而得,已知铁酸盐(MFe2O4)高温还原时,发生反应的MFe2O4与H2的物质的量之比为2∶1,则还原产物MFe2Ox中x= 。MFe2Ox中,+2价铁与+3价铁的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将等质量的铜片、银片、铁片、铝片分别置于四个小烧杯中,然后分别加足量的浓硝酸,放出NO2气体最多的是( )
A.铜片 B.银片 C.铁片 D.铝片
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W四钟元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z、W四种元素的名称:
X 、Y 、Z 、W
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为 ______、_____________________
(3)由X、Y、Z所形成的离子化合物是 ,它与W的最高氧化物的水化物的浓溶液加热时反应的离子方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com