
 反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:
反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:分析 (1)图中反应物能量大于生成物能量;
(2)根据外界条件对速率的影响分析,升温、增大压强、增大浓度、加入催化剂会加快反应速率,但注意常温下铁在浓硫酸中钝化;
(3)铜、铁、稀硫酸构成的原电池中,铁易失电子作负极,铜作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应.
解答 解:(1)从图象可知,反应物总能量高于生成物总能量,所以该反应为放热反应,
故答案为:放热;
(2)A.改铁片为铁粉,增大了接触面积,反应速率增大,故A正确;
B.常温下铁在浓硫酸中钝化不能继续发生反应,故B错误;
C.升高温度,反应速率增大,故C正确;
故答案为:AC;
(3)铜、铁、稀硫酸构成的原电池中,铁易失电子发生氧化反应而作负极,负极上电极反应式为Fe-2e-=Fe2+;铜作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,
故答案为:正;2H++2e-=H2↑.
点评 本题考查了化学反应能量变化、影响化学反应速率因素分析、原电池原理的分析判断,属于基础知识的考查,题目难度不大.


科目:高中化学 来源: 题型:多选题

| A. | a点时溶液的pH=7 | |
| B. | c点时的溶质是(NH3•H2O) | |
| C. | b点时溶液中c(NH4+)>c(NH3•H2O) | |
| D. | a~c段参与反应的离子有H+、OH-、Ba2+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制取乙烯 | |
| B. | 乙酸与乙醇在浓硫酸和加热条件下的酯化反应 | |
| C. | 葡萄糖与银氨溶液反应 | |
| D. | 乙醛和氢气的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 试剂 |
| A | FeCl2 | CuCl2 | 铁粉 |
| B | CO2 | HCl | 氢氧化钠溶液 |
| C | NaCl | Na2CO3 | 稀硫酸 |
| D | CuO粉 | Cu | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaCl、Na2CO3、Ba(NO3)2、H2SO4 | B. | BaCl2、CuSO4、NaOH、NaCl | ||
| C. | NaCl、NaOH、H2SO4、Ba(NO3)2 | D. | K2SO4、BaCl2、K2CO3、KNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极,被还原 | B. | 正极,被氧化 | C. | 负极,被还原 | D. | 负极,被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1×10-10mol•L-1 | B. | 1×10-8mol•L-1 | C. | 1×10-4mol•L-1 | D. | 1×10-6mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
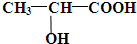
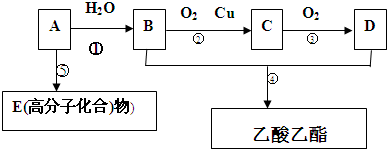
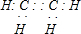
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  的系统命名法为2,5-二甲基-4-乙基己烷 的系统命名法为2,5-二甲基-4-乙基己烷 | |
| B. | 全降解塑料(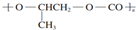 )可由单体环氧丙烷( )可由单体环氧丙烷(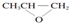 )和CO2加聚制得 )和CO2加聚制得 | |
| C. | 1mol乙酰水杨酸(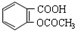 )最多可以和2molNaOH反应 )最多可以和2molNaOH反应 | |
| D. | 油脂、淀粉、蛋白质等高分子化合物都属于混合物,一定条件下均可发生水解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com