
Ä³ŃŠ¾æŠ”×éĪŖĮĖĢ½¾æ¼×ĶéŗĶĀČĘų·“Ó¦µÄĒéæö£¬Éč¼ĘĮĖ¼øøöŹµŃ锣ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ
”¾ŹµŃéŅ»”æÓĆČēĶ¼ĖłŹ¾×°ÖĆ£¬ŹÕ¼ÆŅ»ŹŌ¹Ü¼×ĶéŗĶĀČĘųµÄ»ģŗĻĘųĢ壬ÕÕŗó¹Ū²ģµ½ĮæĶ²ÄŚŠĪ³ÉŅ»¶ĪĖ®Öł£¬ČĻĪŖÓŠĀČ»ÆĒāÉś³É”£
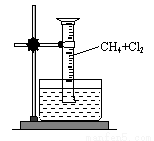
£Ø1£©øĆ·“Ó¦µÄ·“Ó¦ĄąŠĶĪŖ
£Ø2£©øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ØÖ»Š“µŚŅ»²½£© £»
£Ø3£©Ė®²ŪÖŠŹ¢·ÅµÄŅŗĢåÓ¦ĪŖ £»£ØĢī±źŗÅ£©
A£®Ė® B£®±„ŗĶŹÆ»ŅĖ® C£®±„ŗĶŹ³ŃĪĖ® D£®±„ŗĶNaHCO3ČÜŅŗ
”¾ŹµŃ鶞”æŹÕ¼ÆŅ»ŹŌ¹Ü¼×ĶéŗĶĀČĘųµÄ»ģŗĻĘųĢ壬¹āÕÕ·“Ó¦ŗ󣬵Ī¼ÓAgNO3ČÜŅŗ£¬æ“µ½ÓŠ°×É«³ĮµķÉś³É£¬ČĻĪŖÓŠĀČ»ÆĒāÉś³É”£
£Ø4£©ÄćČĻĪŖøĆŹµŃéÉč¼ĘµĆ³öµÄ½įĀŪŹĒ·ńÕżČ·µÄ £¬
Čō²»ÕżČ·£¬ĄķÓÉŹĒ£ŗ
”¾ŹµŃéČż”æ
²½ÖčŅ»£ŗŹÕ¼Æ°ėŹŌ¹ÜĀČĘų£¬¼ÓČė10 mLÕōĮóĖ®£¬³ä·ÖÕńµ“£¬²ÉÓĆDISĻµĶ³µÄpH“«øŠĘ÷²āČÜŅŗµÄpH£ØĻĀĶ¬£©”£²āµĆpH = 3.26
²½Ö趞£ŗŹÕ¼ÆŅ»ŹŌ¹Ü¼×ĶéŗĶĀČĘųµÄ»ģŗĻĘųĢå£Øø÷Õ¼50%£©£¬ŌŚ40 WµÄČÕ¹āµĘĻĀ¹āÕÕ6 minŗ󣬼ÓČė10 mLÕōĮóĖ®£¬³ä·ÖÕńµ“£¬²āµĆpH = 1.00”£
£Ø5£©ÅŠ¶ĻøĆ·“Ó¦ÖŠÓŠĀČ»ÆĒāÉś³ÉµÄŅĄ¾ŻŹĒ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ÄźŗÓ±±¶Ø֯֊ѧ³ŠÖĒ°ąø߶žÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹Ų²ÄĮĻµÄĖµ·ØÖŠ²»ÕżČ·µÄŹĒ£Ø £©”£
A£®“«Ķ³µÄĪŽ»ś·Ē½šŹō²ÄĮĻĖäÓŠ²»ÉŁÓÅµć£¬µ«ÖŹ“ą£¬¾²»ĘšČČ³å»÷
B£®ŠĀŠĶĪŽ»ś·Ē½šŹō²ÄĮĻĖäČ»æĖ·žĮĖ“«Ķ³ĪŽ»ś·Ē½šŹō²ÄĮĻµÄȱµć£¬µ«Ēæ¶Č±Č½Ļ²ī
C£®øßĪĀ½į¹¹²ÄĮĻ¾ßÓŠÄÜÄĶøßĪĀ£¬²»ÅĀŃõ»Æ£¬ÄĶĖį¼īøÆŹ“£¬ĆܶȊ”µČÓŵć
D£®ŠĀŠĶĪŽ»ś·Ē½šŹō²ÄĮĻĢŲŠŌÖ®Ņ»ŹĒ¾ßÓŠ¹āѧĢŲŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗÓ±±Ź”ø߶žĻĀĘŚÄ©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
øßĢśĖįÄĘ£ØNa2FeO4£©¾ßÓŠŗÜĒæµÄŃõ»ÆŠŌ£¬ŹĒŅ»ÖÖŠĀŠĶµÄĀĢÉ«¾»Ė®Ļū¶¾¼Į”£¹¤ŅµÉĻæÉŅŌĶعż“ĪĀČĖįÄĘŃõ»Æ·ØÖʱøøßĢśĖįÄĘ£¬Éś²ś¹ż³ĢČēĶ¼£ŗ
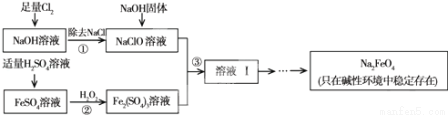
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©¾¹ż²½Öč¢Łŗ󣬼ÓČėNaOH¹ĢĢåµÄŌŅņŹĒ £®
£Ø2£©²½Öč¢Ś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ £®
£Ø3£©“ÓČÜŅŗ¢ńÖŠ·ÖĄė³öNa2FeO4ŗ󣬻¹ÓŠø±²śĘ·Na2SO4”¢NaCl£¬Ōņ²½Öč¢ŪÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ £®
£Ø4£©½«Ņ»¶ØĮæµÄNa2FeO4Ķ¶Čėµ½pH²»Ķ¬µÄĪŪĖ®ÖŠ£ØĪŪĖ®ÖŠĘäÓą³É·Ö¾łĻąĶ¬£©£¬ČÜŅŗÖŠNa2FeO4ÅØ¶Č±ä»ÆČēĶ¼ĒśĻߢń”¢¢ņĖłŹ¾£¬ŹŌĶĘ²āĒśĻߢń±ČĒśĻߢņ¶ŌÓ¦µÄĪŪĖ®pH £ØĢī”°øß”±»ņ”°µĶ”±£©£®
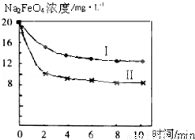
£Ø5£©Ķعż¼ĘĖćµĆÖŖNa2FeO4µÄĻū¶¾Š§ĀŹ£ØŅŌµ„Ī»ÖŹĮæµĆµ½µÄµē×ÓŹż±ķŹ¾£©±ČĀČĘųµÄ £ØĢī”°øß”±»ņ”°µĶ”±£©£¬ÓĆøßĢśĖįÄĘ“śĢęĀČĘų×÷¾»Ė®Ļū¶¾¼ĮµÄÓŵćŹĒ £Ø“š³öĮ½µć¼“æÉ£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗÓ±±Ź”ø߶žĻĀĘŚÄ©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ČēĶ¼W”¢X”¢Y”¢ZĪŖĖÄÖÖĪļÖŹ£¬Čō¼żĶ·±ķŹ¾ÄÜŅ»²½×Ŗ»ÆµÄ³£¼ū·“Ó¦£¬ĘäÖŠÄÜŹµĻÖĶ¼Ź¾×Ŗ»Æ¹ŲĻµµÄŹĒ
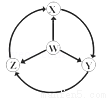
Ń”Ļī | W | X | Y | Z |
A | S | SO2 | SO3 | H2SO4 |
B | Na | Na2O2 | NaOH | NaCl |
C | Fe | FeCl3 | Fe(OH)2 | FeCl2 |
D | Al | AlCl3 | NaAlO2 | Al2(SO4)3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗÓ±±Ź”ø߶žĻĀĘŚÄ©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚĢ½¾æSO2ŠŌÖŹµÄŹµŃéÖŠ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®SO2ĘųĢåĶØČėNaOHČÜŅŗÖŠ£¬²śÉśµ¹ĪüĻÖĻó£¬ĖµĆ÷SO2¼«Ņ×ČÜÓŚĖ®
B£®½«SO2ĶØČėBaCl2 ČÜŅŗÖŠÖĮ±„ŗĶ£¬ĪŽ³Įµķ²śÉś£¬ŌŁĶØČėCl2£¬²śÉś°×É«³Įµķ
C£®SO2ĘųĢåĶØČėäåĖ®ÖŠ£¬äåĖ®µÄŃÕÉ«ĶŹČ„£¬ĖµĆ÷SO2¾ßÓŠĘư׊Ō
D£®SO2ĘųĢåĶØČėBa(NO3)2ČÜŅŗÖŠ£¬ČÜŅŗ³öĻÖ»ė×ĒĻÖĻó£¬ĖµĆ÷ÓŠBaSO3³ĮµķÉś³É
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ¹ćĪ÷¹šĮÖŹ®°ĖÖŠø߶žÉĻæŖŃ§æ¼ŹŌ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ijӊ»śĪļµÄ½į¹¹¼ņŹ½ČēĻĀ,¹ŲÓŚøĆÓŠ»śĪļµÄĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
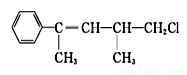
A£®²»ÄÜŹ¹KMnO4ĖįŠŌČÜŅŗĶŹÉ«
B£®ÄÜŹ¹äåĖ®ĶŹÉ«
C£®ŌŚ¼ÓČČŗĶ“߻ƼĮ×÷ÓĆĻĀ,×ī¶ąÄÜÓė4 mol H2·“Ó¦
D£®Ņ»¶ØĢõ¼žĻĀ,ÄÜ·¢ÉśČ”“ś·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ¹ćĪ÷¹šĮÖŹ®°ĖÖŠø߶žÉĻæŖŃ§æ¼ŹŌ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A£®±ūĻ©µÄ½į¹¹¼ņŹ½ĪŖCH2CHCH3
B£®ŠĀĪģĶéµÄ¶žĀČ“śĪļÓŠ2ÖÖ
C£®·Ö×ÓŹ½ĪŖCH4OŗĶC2H6OµÄĪļÖŹŅ»¶Ø»„ĪŖĶ¬ĻµĪļ
D£®¼üĻߏ½ĪŖ µÄÓŠ»śĪļµÄ·Ö×ÓŹ½ĪŖC8H10
µÄÓŠ»śĪļµÄ·Ö×ÓŹ½ĪŖC8H10
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ¹ćĪ÷¹šĮÖŹ®°ĖÖŠøßŅ»ÉĻæŖŃ§æ¼ŹŌ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖ£ŗŌŚ273K£¬101KpaµÄĢõ¼žĻĀ£¬Ä³ĘųĢå£ŗ¢ŁÖŹĮæĪŖm£¬¢ŚĻą¶Ō·Ö×ÓÖŹĮæĪŖM£¬¢ŪĢå»żĪŖV£¬¢ÜĆܶČĪŖ¦Ń£¬¢ŻĖłŗ¬·Ö×ÓŹżĪŖN£Ø°¢·ü¼ÓµĀĀŽ³£ŹżĪŖNA£©£¬ĶعżŅŌÉĻĢõ¼žĪŽ·ØĒó³öøĆĘųĢåĪļÖŹµÄĮæ
µÄŹĒ£Ø £©
A£®¢Ł¢Ś B£®¢Ū C£®¢Ż D£®¢Ś¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ¼ŖĮÖŹ”øßČżÉĻµŚŅ»“Ī½×¶Ī²ā»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
¶ž¼Ūøõ²»ĪȶØ, ¼«Ņ×±»ŃõĘųŃõ»Æ”£“×ĖįŃĒøõĖ®ŗĻĪļ{ [Cr(CH3COO)2]2”¤2H2O£¬Ļą¶Ō·Ö×ÓÖŹĮæĪŖ376£żŹĒŅ»ÖÖÉīŗģÉ«¾§Ģ壬²»ČÜÓŚĄäĖ®ŗĶĆŃ£¬Ņ×ČÜÓŚŃĪĖį£¬ŹĒ³£ÓƵÄŃõĘųĪüŹÕ¼Į”£ŹµŃéŹŅÖŠŅŌŠæĮ£”¢CrCl3ČÜŅŗ”¢“×ĖįÄĘČÜŅŗŗĶŃĪĖįĪŖÖ÷ŅŖŌĮĻÖʱø“×ĖįŃĒøõĖ®ŗĻĪļ£¬Ęä×°ÖĆČēĻĀĶ¼ĖłŹ¾£ŗ

 Öʱø¹ż³ĢÖŠ·¢ÉśµÄ·“Ó¦ČēĻĀ£ŗ
Öʱø¹ż³ĢÖŠ·¢ÉśµÄ·“Ó¦ČēĻĀ£ŗ
Zn(s) + 2HCl(aq) = ZnCl2(aq) + H2(g)£»
2CrCl3(aq)  + Zn(s)= 2CrCl2 (aq) + ZnCl2(aq)
+ Zn(s)= 2CrCl2 (aq) + ZnCl2(aq)
2Cr2+(aq) + 4CH3COO”Ŗ(aq) + 2H2O(l) = [Cr(CH3COO)2]2”¤2H2O (s)
Ēė»Ų“š ĻĀĮŠĪŹĢā£ŗ
ĻĀĮŠĪŹĢā£ŗ
(1)ŅĒĘ÷1µÄĆū³ĘŹĒ , ĖłŹ¢×°µÄŹŌ¼ĮŹĒ ”£
(2)±¾ŹµŃéÖŠĖłÓƵÄČÜŅŗ£¬ÅäÖĘÓƵÄÕōĮóĖ®¶¼ŠčŹĀĻČÖó·Š£¬ŌŅņŹĒ ”£
(3)ŹµŃéæŖŹ¼Éś³ÉH2Ęųŗó, ĪŖŹ¹Éś³ÉµÄCrCl2ČÜŅŗÓėCH3COONaČÜŅŗĖ³Ąū»ģŗĻ£¬Ó¦ ·§ĆÅA”¢ ·§ĆÅB (Ģī”°“ņæŖ”±»ņ”°¹Ų±Õ”±)”£
(4)±¾ŹµŃéÖŠŠæĮ£Šė¹żĮ棬ĘäŌŅņŹĒ £¬ ”£
(5)ŅŃÖŖĘäĖü·“Ó¦Īļ×ćĮ棬ŹµŃ鏱ȔÓƵÄCrCl3ČÜŅŗÖŠŗ¬ČÜÖŹ6.34 g£¬ŹµŃéŗóµĆøÉŌļ“æ¾»µÄ[Cr(CH3COO)2]2”¤2H2O 5.64 g£¬Ēė¼ĘĖćøĆŹµŃéĖłµĆ²śĘ·µÄ²śĀŹ ”£
(6)ČōŹ¹ÓĆøĆ×°ÖĆÖʱøFe(OH)2£¬ĒŅÄܽĻ³¤Ź±¼ä擵½Fe(OH)2°×É«³ĮµķĻÖĻó”£ŌņŌŚ1”¢2”¢3֊ӦװČėµÄŹŌ¼ĮŅĄ“ĪĪŖ ”¢ ”¢ ”£(Š“»ÆѧŹ½)
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com