
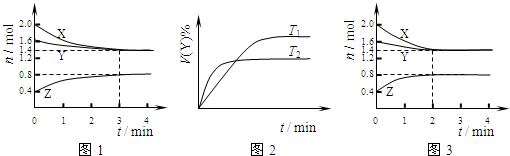
(1)在密闭容器中进行下列反应:M(g) + N(g) R(g) + 2L(?) ,此反应规律符合下图图像。
R(g) + 2L(?) ,此反应规律符合下图图像。

①T1 T2 ,正反应的△H 0。(填“>”、“<”或“=”,下同)。
②P1 P2 , L为 。(填“固”或“液”或“气”态)。
(2)合成氨的原理为:N2(g)+3H2(g)  2NH3(g)
2NH3(g)  H=-92.4 kJ/mol,该反应的能量变化如图所示。
H=-92.4 kJ/mol,该反应的能量变化如图所示。

①在反应体系中加入催化剂,反应速率增大,E2的变化是 (填“增大”、“减小”或“不变”)。②若在一密闭容器中加入1molN2和3molH2,在一定条件下充分反应,放出的热量 92.4kJ.(填“>”、“<”或“=”)。
③将1 mol N2和3 mol H2充入体积不变的密闭容器中,在一定条件下达到平衡,此时欲提高该容器中H2的转化率,下列措施可行的是 (填字母)。
A.向容器中按原比例再充入原料气 B.向容器中再充入一定量H2
C.改变反应的催化剂 D.液化生成物分离出氨
④若在密闭容器中充入2molN2和6molH2反应达平衡时N2的转化率为40%。若以NH3作为起始反应物,反应条件与上述反应相同时,要使其反应达到平衡时各组分的物质的量分数与前者相同,则NH3的起始物质的量和它的转化率分别为 mol、 。
(共12分)(1)①<、< ②<、气态 (2)①减小 ②<(以上各1分)
③AD ④4、60%(以上各2分)
【解析】
试题分析:(1)①根据图像可知,当压强均为P1时,温度为T2的曲线首先达到平衡状态,这说明温度是T2>T1。但温度高,R的含量低,这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应,即△H<0。
②根据图像可知,当温度均为T1时,压强为P2的曲线首先达到平衡状态,这说明P2>P1。但压强高,R的含量低,这说明增大越强平衡向逆反应方向移动,因此正方应是体积增大的可逆反应,即L一定是气态。
(2)①催化剂能降低反应的活化能,但不能改变反应热,所以在反应体系中加入催化剂,反应速率增大。由于E1减小,反应热不变,所以E2的变化一定是减小。
②由于该反应是可逆反应,因此若在一密闭容器中加入1molN2和3molH2,不可能生成2mol氨气,因此在一定条件下充分反应,放出的热量<92.4kJ。
③A、向容器中按原比例再充入原料气,相当于增大压强,平衡向正反应方向移动,氢气的转化率增大,A正确;B、向容器中再充入一定量H2,平衡向正反应方向,但氢气转化率降低,B不正确;C、改变反应的催化剂,反应速率变化,平衡状态不变,则氢气的转化率不变,C不正确;D、液化生成物分离出氨,降低生成物浓度,平衡向正反应方向移动,氢气的转化率增大,D正确,答案选AD。
④若在密闭容器中充入2molN2和6molH2反应达平衡时N2的转化率为40%。若以NH3作为起始反应物,反应条件与上述反应相同时,要使其反应达到平衡时各组分的物质的量分数与前者相同,这说明平衡应该是等效的。由于温度和容器容积不变,则氨气的物质的量完全转化为氮气和氢气应该是2mol和6mol,所以需要氨气的物质的量是4mol;平衡时生成氨气的物质的量是2mol×40%×2=1.6mol,因此如果从4mol氨气开始建立平衡状态,则氨气的转化率是= ×100%=60%。
×100%=60%。
考点:考查外界条件对平衡状态的影响、图像识别;反应热与转化率的有关计算以及等效平衡的应用等


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
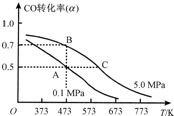 (2013?无锡一模)天然气、煤炭气(CO、H2)的研究在世界上相当普遍.其中天然气和二氧化碳可合成二甲醚,二甲醚与水蒸气制氢气作为燃料电池的氢能源,比其他制氢技术更有优势.主要反应为:
(2013?无锡一模)天然气、煤炭气(CO、H2)的研究在世界上相当普遍.其中天然气和二氧化碳可合成二甲醚,二甲醚与水蒸气制氢气作为燃料电池的氢能源,比其他制氢技术更有优势.主要反应为:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CH3OCH3、1mol H2O | 2mol CH3OH | 1mol CH3OH |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 吸收a kJ | 放出b kJ | 放出c kJ |
| 平衡时体积(L) | V1 | V2 | V3 |
| 反应物转化率 | α 1 | α 2 | α 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省无锡市高三上学期期末考试化学试卷(解析版) 题型:填空题
天然气、煤炭气(CO、H2)的研究在世界上相当普遍。其中天然气和二氧化碳可合成二甲醚,二甲醚与水蒸气制氢气作为燃料电池的氢能源,比其他制氢技术更有优势。主要反应为:
①CH3OCH3(g)
+H2O(g) 2CH3OH(g) △H=
37Kj·mol-1
2CH3OH(g) △H=
37Kj·mol-1
②CH3OH(g)+H2O(g)
 3 H2(g)+CO2(g) △H =49Kj·mol-1
3 H2(g)+CO2(g) △H =49Kj·mol-1
③CO2(g)
+H2(g)  CO(g)
+H2O(g) △H=41.3Kj·mol-1
CO(g)
+H2O(g) △H=41.3Kj·mol-1
其中反应③是主要的副反应,产生的CO对燃料电池Pt电极有不利影响。
请回答下列问题:
(1)二甲醚可以通过天然气和CO2合成制得,该反应的化学方程式为 。
(2)CH3OCH3(g)与水蒸气制氢气的热化学方程式为 。
(3)下列采取的措施和解释正确的是 。(填字母序号)
A.反应过程在低温进行,可减少CO的产生
B.增加进水量,有利于二甲醚的转化,并减少CO的产生
C.选择在高温具有较高活性的催化剂,有助于提高反应②CH3OH的转化率
D.体系压强升高,虽然对制取氢气不利,但能减少CO的产生
(4)煤炭气在一定条件下可合成燃料电池的另一种重要原料甲醇,反应的化学方程式为:
CO (g) +2H2(g)  CH3OH(g)
△H <0。现将l0mol CO与20mol H2置于密闭容器中,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(
CH3OH(g)
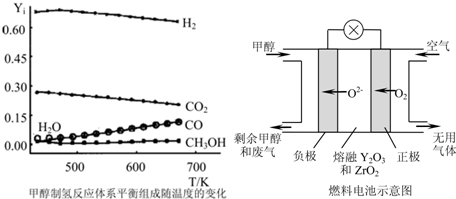
△H <0。现将l0mol CO与20mol H2置于密闭容器中,在催化剂作用下发生反应生成甲醇,CO的平衡转化率( )与温度、压强的关系如下图所示。
)与温度、压强的关系如下图所示。

①自反应开始到达平衡状态所需的时间tA tB(填“大于”、“小于”或“等于”)。
②A、C两点的平衡常数KA KC(填“大于”、“小于”或“等于”)。
(5)某工作温度为650oC的熔融盐燃料电池,是以镍合金为电极材料,负极通人煤炭气(CO、H2),正极通人空气与CO2的混合气体,用一定比例的Li2CO3和Na2CO3混合物做电解质。请写出正极的电极反应式 ____ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com