
【题目】硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示。下列说法正确的是( )

A.m=2
B.在Xm-中,硼原子轨道的杂化类型相同
C.1、2原子间和4、5原子间的化学键可能是配位键
D.Xm-中含离子键和配位键
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】热催化合成氨面临的两难问题是:釆用高温增大反应速率的同时会因平衡限制导致NH3产率降低。我国科研人员研制了TiHFe双温区催化剂(Ti-H区域和Fe区域的温度差可超过100℃)。Ti-H-Fe双温区催化合成氨的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是( )
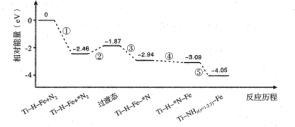
A.①为氮氮三键的断裂过程
B.①②③在低温区发生,④⑤在高温区发生
C.使用Ti-H-Fe双温区催化剂使合成氨反应转变为吸热反应
D.④为N原子由Fe区域向Ti-H区域的传递过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组欲测定市售橙汁饮料中维生素C的含量。每100克鲜榨橙汁中含有大约37.5毫克的维生素C。实验室可用碘量法测定橙汁饮料中维生素C的含量,反应的方程式为C6H8O6+I2==C6H6O6+2HI(维生素C化学式为C6H8O6,相对分子质量为176),其实验步骤及相关数据如下:
①标准溶液的稀释:移取浓度为0.0080mol/L的碘标准溶液25.00mL于250mL容量瓶中,定容,摇匀备用。
②移取10.00mL饮料样品(设密度为1.0g/cm3)于250 mL锥形瓶中,加入50mL蒸馏水,2mL指示剂。
③在滴定管中装入稀释后的标准溶液,滴定至终点,读取并记录相关数据。
④重复测定3次,数据记录如下表。
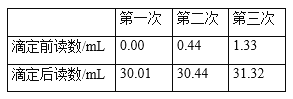
回答下列问题:
(1)实验中盛装标准溶液应选择______(填“酸式”或“碱式”)滴定管。
(2)步骤2中加入的指示剂是___________,判断滴定达到终点的现象是__________。
(3)实验中下列操作可能导致测定结果偏低的是_______(填标号)。
A.稀释标准溶液定容时俯视刻度线
B.滴定结束时俯视读
C.在锥形瓶中加入样品后放置较长时间才开始滴定
D.滴定管尖嘴部分有气泡,滴定后消失
(4)计算该饮料样品中维生素C含量为________mg/100 g。该含量______(填“高于”或“低于”)鲜榨橙汁。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH固体分别加入浓度均为0.1 mol·L-1、体积均为100 mL的两种一元酸HX、HY的溶液中,lg![]() 随加入NaOH的物质的量的变化情况如图所示。下列叙述正确的是( )
随加入NaOH的物质的量的变化情况如图所示。下列叙述正确的是( )
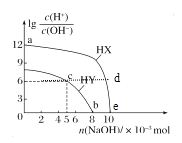
A.由a点到e点水的电离程度先增大后减小
B.d点溶液中存在:c(HX)+c(X-)=0.1mol/L
C.c点溶液中存在:c(Y-)+2c(OH-)=2c(H+)+c(HY)
D.b点溶液中存在:c(HY)+c(Na+)=0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸橙花酯兼有橙花和玫瑰花香气,其结构简式如图。关于该有机物的叙述中正确的是
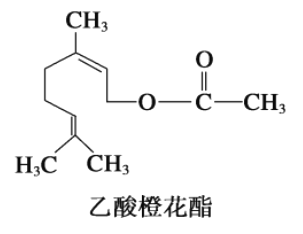
① 在Ni催化条件下1mol该有机物可与3mol H2发生加成;
② 该有机物不能发生银镜反应;
③ 该有机物分子式为C12H22O2;
④ 该有机物的同分异构体中不可能有酚类;
⑤ 1 mol该有机物水解时只能消耗1 mol NaOH
A. ②③④ B. ①④⑤ C. ②④⑤ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤代烃是一类重要的有机合成中间体,是许多有机合成的原料.根据卤代烃的相关性质,回答下列问题.
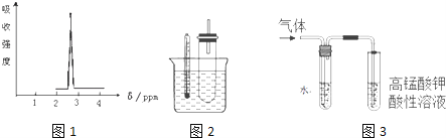
(1)化合物A的分子式是C3H6Br2,A的氢核磁共振氢谱图如图1所示,则A的结构简式为___________.
(2)某同学用如图2装置(铁架台、酒精灯等略)验证取代反应和消去反应的产物
实验操作Ⅰ:在试管中加入5mL1mol/LNaOH溶液和0.5mL溴乙烷振荡.
实验操作Ⅱ:将试管如图2固定后,水浴加热.
①据图1:用水浴加热而不直接用酒精灯加热的原因2是________.
②图3是为证明溴乙烷在NaOH乙醇溶液中加热发生的是消去反应.
i实验中需要检验的产物是_______,水的作用是__________,实验现象是_________________.
ii若将“酸性高锰酸钾溶液”换成“Br2的CCl4溶液”,还需要装水的洗气装置吗________?(填“需要”或“不需要”),理由是________.
iii所检验的产物与Br2的CCl4溶液反应的化学方程式为___________.
(3)已知:
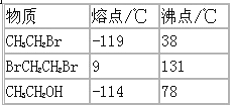
分离溴乙烷与1,2-二溴乙烷混合气体的方法是____________.
a.冰水浴冷却→过滤
b.水浴冷却→蒸馏
c.冰水浴冷却→加水萃取→分液
d.水浴冷却→加水萃取→分液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2一元弱酸)和氟硼酸(HBF4)均可用于植物杀菌。常温时,有1molL-1的H3PO2溶液和1molL-1的HBF4溶液,两者起始时的体积均为V0,分别向两溶液中加水,稀释后溶液的体积均为V,两溶液的pH变化曲线如图所示。下列说法错误的是
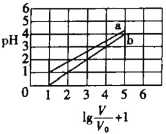
A.常温下,NaBF4溶液的pH=7
B.常温下,H3PO2的电离平衡常数约为1.1![]() 10-2
10-2
C.NaH2PO2 溶液中:c(Na+) =c( H2PO2- ) +c( HPO22-) +c(PO23-) +c( H3PO2)
D.常温下,在0≤pH≤4时,HBF4溶液满足![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
晶体硼(其每个结构单元中有12个B原子) | NaCl | S8 | HCN | |
结构模型示意图 |
|
|
|
|
备注 | 熔点2573K | —— | 易溶于CS2 | —— |
A.晶体硼属于原子晶体,结构单元中含有30个B-B键,含20个正三角形
B.NaCl晶体中每个Na+周围距离最近且相等的Na+有6个
C.S8分子中的共价键为非极性键
D.HCN分子中含有2个σ键,2个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,是某种有机物分子的球棍模型图。图中的“棍”代表单键或双键,不同大小的“球”代表三种不同的短周期元素的原子。对该有机物的叙述不正确的是
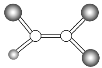
A.该有机物可能的分子式为C2HCl3
B.该有机物的分子中一定有碳碳双键
C.该有机物分子中的所有原子在同一平面上
D.该有机物分子中形成的化学键都是极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com