
短周期元素A、B、C、D、E的原子序数依次增大,其中B和E同主族。A元素的最高正价和最低负价的绝对值之差为2;1molC单质能与冷水反应,在标准状况下生成11.2LH2;D原子最外层电子数等于其周期序数;E-的电子层结构与Ar原子相同。
(1)D原子结构示意图为____________;B和C形成的化合物的电子式为___________;
(2 )B、C、D简单离子的半径大小为__________;(用离子符号和“>”、“=”或“<”表示);
(3)①写出单质铜与元素A的最高价氧化物对应水化物的稀溶液反应的化学方程式为 。
②写出E单质与C的最高价氧化物的水化物的溶液反应的离子方程式为 。
(4)元素非金属性强弱比较有很多方法,其中B和E的非金属性强弱的研究方案中不可行的是
_________(填序号);
A.比较两种单质的颜色 B.比较氢化物的稳定性
C.依据两元素在周期表的位置 D.比较原子半径大小
E.比较最高价氧化物对应水化物的酸性
科目:高中化学 来源:2016届福建师大附中高三下学期模拟考试理综化学试卷(解析版) 题型:简答题
【化学——选修3:物质结构与性质】
物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
(1)第二周期中,元素的第一电离能处于B与N之间的元素有_________种。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为_________________。
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是_____________,1mol(C2H5O)3P=O分子中含有的σ键的数目为__________________。
(4)已知固态NH3、H2O、HF的氢键键能和结构如下:
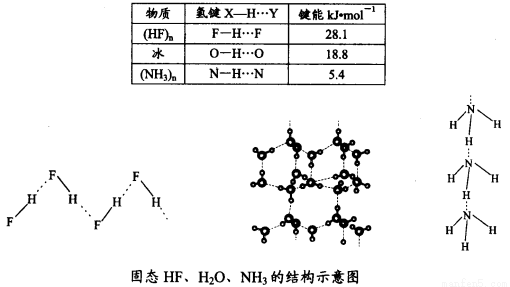
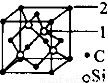
解释H2O、HF、NH3沸点依次降低的原因___________________。
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有___________个,与碳原子等距离最近的碳原子有__________个。已知碳化硅晶胞边长为apm,则晶胞图中1号硅原子和2号碳原子之间的距离为________pm,碳化硅的密度为__________g/cm3。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:填空题
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小,请回答下列问题:
(1)FeCl3净水的原理是 ,FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) ;
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10﹣2mol•L﹣1,c(Fe3+)=1.0×10﹣3mol•L﹣1,c(Cl﹣)=5.3×10﹣2mol•L﹣1,则该溶液的pH约为 ;
②完成NaClO3氧化FeCl2的离子方程式:
ClO3﹣+ Fe2++ = Cl﹣+ Fe3++ 。
(3)FeCl3在溶液中分三步水【解析】
Fe3++H2O Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)2++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:选择题
在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发 生反应:H2(g)+Br2(g) 2HBr(g)△H<0. 当温度分别为T1、T2,平衡时, H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法正确的是( )
2HBr(g)△H<0. 当温度分别为T1、T2,平衡时, H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法正确的是( )
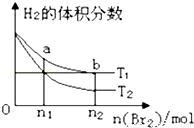
A.由图可知:T2>T1
B.a、b两点的反应速率:b>a
C.为了提高Br2(g)的转化率,可采取增加Br2 (g)通入量的方法
D.T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:选择题
下列各组热化学方程式中,化学反应的△H1大于△H2的是( )
①C(s)+O2(g)═CO2(g)△H1; C(s)+ O2(g)═CO(g)△H2
O2(g)═CO(g)△H2
②2H2(g)+O2(g)═2H2O(g)△H1; 2H2(g)+O2(g)═2H2O(l)△H2
③H2(g)+Cl2(g)═2HCl(g)△H1;  H2(g)+
H2(g)+ l2(g)═HCl(g)△H2
l2(g)═HCl(g)△H2
④CaCO3(s)═CaO(s)+CO2(g)△H1; CaO(s)+H2O(l)═Ca(OH)2(s);△H2.
 WA.①③ B.①④ C.②④ D.②③
WA.①③ B.①④ C.②④ D.②③

查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州遵义航天高中高一下期中理综化学试卷(解析版) 题型:选择题
下面表格中的实验操作、实验现象和结论均正确且相符的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸只表现脱水性 |
B | 将盐酸滴入Na2CO3溶液中 | 有气泡产生 | 氯的非金属性比碳强 |
C | 向某溶液中加入浓NaOH溶液并加热,在试管口用湿润的红色石蕊试纸检验 | 试纸变蓝 | 原溶液中含有NH4+ |
D | SO2通入品红溶液中 | 溶液褪色 | SO2具有还原性 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州遵义航天高中高二下期中理综化学试卷(解析版) 题型:填空题
某烃A 0.2 mol 在氧气中完全燃烧后,生成CO2和H2O各1.2 mol。试回答:
(1)烃A的分子式为_____________。
(2)若取一定量的烃A完全燃烧后,生成CO2和H2O各3 mol,则有________g烃A参加了反应,燃烧时消耗标准状况下的氧气___________L。
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为__________________。
(4)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,烃A可能有的结构简式为__________________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二下期中化学试卷(解析版) 题型:实验题
氧化铁黄(化学式为FeOOH)是一种黄色颜料,工业上用废铁为主要原料生产氧化铁黄的一种工艺流程如下:
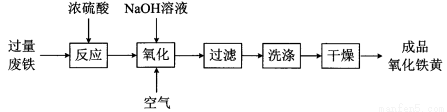
(1)氧化铁黄中铁元素的化合价为 ,废铁在反应前常用热的纯碱溶液清洗表面油污,其原理是 (写离子方程式)。
(2)氧化过程生成氧化铁黄的化学方程式是 。
(3)上述流程中,检验“洗涤”是否完全的方法是 。
(4)氧化时应控制pH的合理范围是3.5-4.0,pH过小导致氧化铁黄产率较低的可能原因是 。
(5)取1g样品进行纯度测试,将其溶解于足量稀盐酸中,后用一定浓度的过量NaOH溶液沉淀其中的铁元素,得到沉淀的质量为Bg,试用所给数据求出产品的纯度 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一下期中化学试卷(解析版) 题型:选择题
下列不能使有色布条褪色的物质是
A.氯水 B.次氯酸钠溶液 C.漂白粉溶液 D.氯化钙溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com