
【题目】判断下列粒子的空间构型
(1)CO2:_______________________
(2)H2S:____________
(3)SO2:___________
(4)NH4+:_________________
(5)CO32-:_____________
【答案】 直线形 V形 V形 正四面体形 平面三角形
【解析】用价层电子对互斥理论判断,CO2为直线形,H2S为V形,SO2为V形,NH4+为正四面体形,CO32-为平面三角形。
(1)CO2中中心原子C上的孤电子对数为![]() (4-2
(4-2![]() 2)=0,成键电子对数为2,价层电子对数为0+2=2,VSEPR模型为直线形,C原子没有孤电子对,CO2为直线形。
2)=0,成键电子对数为2,价层电子对数为0+2=2,VSEPR模型为直线形,C原子没有孤电子对,CO2为直线形。
(2)H2S中中心原子S上的孤电子对数为![]() (6-2
(6-2![]() 1)=2,成键电子对数为2,价层电子对数为2+2=4,VSEPR模型为四面体形,略去S原子上的两对孤电子对,H2S为V形。
1)=2,成键电子对数为2,价层电子对数为2+2=4,VSEPR模型为四面体形,略去S原子上的两对孤电子对,H2S为V形。
(3)SO2中中心原子S上的孤电子对数为![]() (6-2
(6-2![]() 2)=1,成键电子对数为2,价层电子对数为1+2=3,VSEPR模型为平面三角形,略去S原子上的一对孤电子对,SO2为V形。
2)=1,成键电子对数为2,价层电子对数为1+2=3,VSEPR模型为平面三角形,略去S原子上的一对孤电子对,SO2为V形。
(4)NH4+中中心原子N上的孤电子对数为![]() (5-1-4
(5-1-4![]() 1)=0,成键电子对数为4,价层电子对数为0+4=4,VSEPR模型为正四面体形,N原子没有孤电子对,NH4+为正四面体形。
1)=0,成键电子对数为4,价层电子对数为0+4=4,VSEPR模型为正四面体形,N原子没有孤电子对,NH4+为正四面体形。
(5)CO32-中中心原子C上的孤电子对数为![]() (4+2-3
(4+2-3![]() 2)=0,成键电子对数为3,价层电子对数为0+3=3,VSEPR模型为平面三角形,C原子没有孤电子对,CO32-为平面三角形。
2)=0,成键电子对数为3,价层电子对数为0+3=3,VSEPR模型为平面三角形,C原子没有孤电子对,CO32-为平面三角形。


科目:高中化学 来源: 题型:
【题目】科学家预测,月球的土壤中吸附着数百万吨![]() ,100吨
,100吨![]() 核聚变释放的能量相当于目前人类一年消耗的能量。下列说法正确的是
核聚变释放的能量相当于目前人类一年消耗的能量。下列说法正确的是
A. ![]() 的最外层的最外层电子数为2,具有较强的金属性
的最外层的最外层电子数为2,具有较强的金属性
B. ![]() 位于周期表第一周期第ⅡA族
位于周期表第一周期第ⅡA族
C. 每个氦分子中含有的质子数为2、中子数为1
D. 该原子核中质子数为2、中子数为3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 向水中通入氯气:Cl2+H2O===2H+ + ClO+ Cl
B. 向Ca(HCO3)2溶液中滴加足量NaOH溶液:Ca2+ + 2HCO3+2OH===CaCO3↓+CO32+2H2O
C. 向明矾溶液中加过量氨水:Al3++4NH3·H2O===AlO2+4NH4++2H2O
D. 将Fe2O3溶解与足量HI溶液:Fe2O3+6H+===2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置。A中的化学反应方程式是________________(锰被还原为Mn2+)。
②C中得到紫色固体和溶液。C中Cl2发生的反应有3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,另外还有__________________(写离子方程式)。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否为K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
Ⅰ.由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由____________________________________产生(用离子方程式表示)。
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是________________。
②根据K2FeO4的制备实验得出:氧化性Cl2________FeO42-(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:
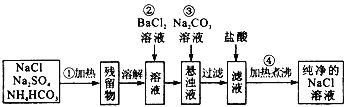
如果此方案正确,那么:
(1)操作①可选择的仪器是_______________。
(2)操作②是否可改为加硝酸钡溶液?_____________;(答“是”或者“否”)理由________________。
(3)进行操作②后,如何判断SO42-已除尽,方法是_____________________。
(4)操作③的目的是___________________。
(5)操作④的目的是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表短周期的一部分:

(1)①表示的元素名称是_________②对应简单离子结构示意图_______。
(2)③位于元素周期表中第________周期,第__________族。
(3)④的单质与 NaOH 溶液反应的离子方程式____________。
(4)⑤在自然界中有质量数为35和37的两种核素,该元素的相对原子质量为35.5,则两核素在自然界中的原子个数之比约为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水FeCl3呈棕红色,极易潮解, 100 ℃ 左右时升华,工业上常用作有机合成催化剂。实验室可用下列装置(夹持仪器略去)制备并收集无水FeCl3。
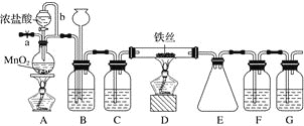
(1)装置A中反应的离子方程式为____________________________________________。
(2)装置F中所加的试剂为________。
(3)导管b的作用为________________________________________________________;
装置B的作用为__________________________________________________________。
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,原因为__________。
(5)反应结束后,拆卸装置前,必须进行的操作是______________________。
(6)为检验所得产品为FeCl3,可进行如下实验:取E中收集的产物少许,加水溶解,向所得溶液中加入
________________________(填试剂名称和现象)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出12种元素在周期表中的位置,按要求回答下列各题:
周期族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ⑦ | ⑨ | ||||||
3 | ② | ④ | ⑥ | ⑧ | ⑩ | |||
4 | ③ | ⑤ |
(1)这12种元素中,化学性质最不活泼的元素是______(填元素符号或化学式,下同),得电子能力最强的原子是______,失电子能力最强的单质与水反应的离子反应方程式是____,常温下单质为液态的非金属单质是____________。
(2)元素⑤的离子结构示意图为__________________。
(3)写出⑦⑧⑨与①形成的简单化合物中最稳定的分子式________。写出⑧⑩两种元素最高价氧化物对应水化物中酸性较弱的化学式________。
(4)写出⑨⑩与①形成的化合物中沸点最低的化学式______酸性最强的化学式_______。
(5)写出④的单质置换出⑦的单质的化学反应方程式:__________________。
②和⑥两种元素最高价氧化物对应的水化物相互反应的离子方程式为__________。
③和⑩两种元素最高价氧化物对应的水化物相互反应的离子方程式为__________。
用电子式表示⑤与⑨组成的二元化合物的形成过程_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com