
| A. | 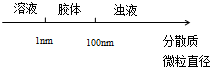 分散系的分类 | B. | 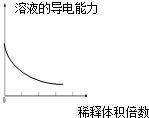 稀释浓氢氧化钠溶液的过程 | ||
| C. | 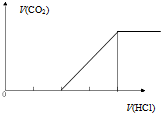 向碳酸钠溶液中逐滴滴加盐酸 | D. |  向偏铝酸钠溶液中逐滴滴加盐酸 |
分析 A.分散质微粒直径在1-100nm直径的为胶体,小于1nm的为溶液,大于100nm的为浊液;
B.溶液的导电能力与离子浓度成正比;
C.碳酸钠和稀盐酸反应先生成碳酸氢钠和NaCl,然后碳酸氢钠再和稀盐酸反应生成NaCl、水和二氧化碳;
D.离子方程式:AlO2-+H++H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O.
解答 解:A.胶体区别于其它分散系的本质特征是胶体粒子直径在1-100nm(10-7~10-9m)之间,溶液的粒子直径小于1nm,浊液的子直径大于100nm,故A正确;
B.稀释浓氢氧化钠溶液,离子的浓度降低,导电能力降低,故B正确;
C.向碳酸钠溶液中逐滴滴加盐酸,先生成碳酸氢钠,再生成氯化钠和二氧化碳,所以先没有二氧化碳生成、后产生二氧化碳,且不产生二氧化碳和二氧化碳完全产生所需稀盐酸体积比为1:1,故C正确;
D.离子方程式:AlO2-+H++H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O,生成沉淀和溶解应为1:3,故D错误;
故选D.
点评 本题考查图象分析,为高频考点,侧重考查学生分析判断能力,明确物质性质、物质分类标准、溶液导电性影响因素是解本题关键,易错选项是C.


 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 钢铁在干燥的环境中不易腐蚀 | |
| B. | 原电池工作时,电解质溶液中的阳离子移向正极 | |
| C. | 用铝质铆钉铆接铁板,铆接处的铁板更易被腐蚀 | |
| D. | 集中回收处理废旧电池的主要目的是防止电池中的重金属离子污染土壤和水源 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
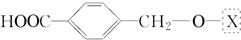 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.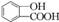 .
. 任意2种.
任意2种.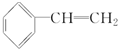 为主要原料制备
为主要原料制备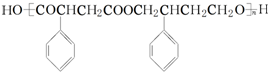 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).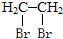
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
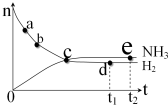 对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),400℃,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示.下列叙述正确的是( )
对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),400℃,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示.下列叙述正确的是( )| A. | 点c处于正反应速率和逆反应速率相等 | |
| B. | 点a的正反应速率比点b的大 | |
| C. | 点d (t1时刻) 和点 e (t2时刻) 处n(N2)不同 | |
| D. | 在t2时刻,正反应速率大于逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+ | |
| B. | 滤纸上有Ag、Cu,滤液中有Ag+、Zn2+、Fe2+ | |
| C. | 滤纸上有Ag、Cu、Fe,滤液中有Cu2+、Zn2+、Fe2+ | |
| D. | 纸上有Ag、Cu、Fe、Zn,滤液中有Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高正价依次降低 | |
| C. | N、O、F原子半径依次增大 | |
| D. | Na、K、Rb的金属性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com