
【题目】A、B、C是与生命活动密切相关的三种常见化合物,每种物质所含元素种类均不超过三种,甲是单质。它们之间有如下转化关系:

化合物D也是生活中常见的化合物,在一定条件下可发生如下反应:D+3甲![]() 3A+2B
3A+2B
请回答下列问题:
(1)在化合物A、B、C、D中所含元素完全相同的是__________和__________(填字母)。
(2)在常温下,A和B通过__________转化为C。该过程的能量转化关系如何?
____________________。
(3)写出由C生成D的反应的化学方程式____________________。
(4)化合物C是人类生命活动不可缺少的物质之一,它在血液中的正常含量是__________。
(5)目前化合物B在大气中含量呈上升趋势,对环境造成的影响是____________________。
【答案】(1)C D(2)绿色植物的光合作用 该过程中光能转化为化学能
(3)CH2OH(CHOH)4CHO![]() 2CH3CH2OH+2CO2↑ (4)100mL血液中约含葡萄糖80—100mg
2CH3CH2OH+2CO2↑ (4)100mL血液中约含葡萄糖80—100mg
(5)温室效应加剧
【解析】
试题A、B、C是与生命活动密切相关的三种常见化合物,每种物质所含元素种类均不超过三值,且甲是单质。因此联系植物的光合作用可知,甲是氧气,C是葡萄糖,A和B是CO2与水。葡萄糖C在一定条件下有分解生成B和化合物D,化合物D也是生活中常见的化合物,燃烧产物是水和CO2,这说明D是乙醇,B是CO2,所以A是水。
(1)在化合物A、B、C、D中所含元素完全相同的是乙醇和葡萄糖,答案选C和D。
(2)在常温下,A和B通过绿色植物的光合作用转化为C。该过程的能量转化关系是光能转化为化学能。
(3)葡萄糖在酶的作用下分解生成乙醇和CO2,反应的化学方程式是CH2OH(CHOH)4CHO![]() 2CH3CH2OH+2CO2↑。
2CH3CH2OH+2CO2↑。
(4)葡萄糖在血液中的正常含量是100mL血液中约含葡萄糖80—100mg。
(5)CO2含量上升,容易引起温室效应。


科目:高中化学 来源: 题型:
【题目】绿色化学、环境保护和人类健康是息息相关的三个主题,请根据已知信息回答有关问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是________(填序号)。
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl→CH3CH2Cl+H2O
C.CH3CH3+Cl2![]() CH3CH2Cl+HCl
CH3CH2Cl+HCl
D.CH2=CHCl+H2![]() CH3CH2Cl
CH3CH2Cl
由上述四个反应可归纳出,原子经济性高的是________反应(填反应类型)。
(2)有毒物质的无害化也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,还可将废水中少量的S2-、NO2-和CN-等有毒有害的还原性酸根离子氧化除去。请写出用ClO2将废水中有剧毒的CN-氧化成无毒气体的离子方程式:____________________并说明该方法的优点:_____________________________________。
(3)如图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图:

活性炭的作用是____________________;用O3消毒的优点是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图①—⑩分别代表有关反应中的一种物质,其中③气体能使酚酞试液变红,⑦是红综色气体,回答:

(1)①中的混合气体通过浓硫酸发生化学反应,主要生成物的化学式是____。
(2)写出碳酸氢铵中阳离子的检验方法______________________________。
(3)写出工业上合成③的化学方程式__________________________________。
(4)⑧与⑨反应的化学方程式是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠、钾与水反应的实验如下图所示:
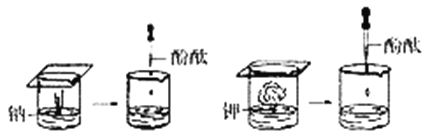
(1)钠、钾与水反应两个实验现象的相同点:
①金属________水面上;
②金属________成闪亮的小球;
③小球四处游动;
④产生嘶嘶的声音;
⑤反应后的溶液使酚酞________。
(2)_______与水反应有轻微的爆鸣声,并很快燃烧起来。
(3)实验结论:________更易与水反应,且反应更_____________________________________。
(4)钾与水反应的化学方程式是___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中碳酸钠的质量分数。
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为____________。
(2)实验中,需加热至恒重的目的是_____________。
[方案二]称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量氢氧化钡溶液,过滤、洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-=BaCO3↓+H2O)。
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为__________。
(2)实验中判断沉淀是否完全的方法是__________。
[方案三]按如下图所示装置进行实验:

(1)D装置的作用是________,分液漏斗中_____(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80g,则样品中碳酸钠的质量分数为________。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21。下列说法不正确的是
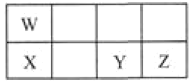
A.W、Y两种元素都能与氧元素形成化合物WO2、YO2
B.原子半径大小:Y<X
C.W元素的单质能从X的某种化合物中置换出X单质
D.氧化物对应水化物的酸性:W<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲配制480 mL物质的量浓度为0.1mol·L-1的CuSO4溶液。
(1)完成该实验用到的仪器主要有:托盘天平、胶头滴管、烧杯、玻璃棒、药匙和____________。
(2)写出整个实验简单的操作过程:计算→称量→溶解→转移→____________→定容→摇匀。
(3)如果用CuSO4固体来配制,应该称量固体的质量为_________________;如果用CuSO4·5H2O来配制,应该称量固体的质量为____________________。
(4)下列操作使配制的溶液浓度偏低的是__________________。
A.配制的过程中有少量的液体溅出烧杯。
B.使用前容量瓶用蒸馏水洗涤,且没有干燥。
C.定容时俯视液面。
D.定容摇匀后,液面下降,又加水至刻度线。
(5)取配制好的溶液50 mL用水稀释到100 mL所得溶液中Cu2+的物质的量浓度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用正盐X(三种常见元素组成的纯净物,摩尔质量为270g/mol)进行如下实验:

步骤②是工业生产制备某种常见试剂的重要环节。实验中观测到:丙能使带火星的木条复燃;乙和丁均为纯净物,且含有相同元素,焰色反应透过蓝色钴玻璃呈紫色;在步骤③中,恰好完全反应时消耗丁7.9g。
请回答:
(1)X的化学式是________,步骤③的化学方程式是________。
(2)X在Ag+的催化作用下能和Mn2+反应,可观察到溶液由无色变紫红色,写出对应的离子方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林是常见的解热镇痛药,结构简式如图所示,有关阿司匹林的说法不正确的是( )

A.能发生水解、酯化、取代、还原反应
B.阿司匹林分子中最多可以有20个原子在同一平面上
C.1mol该物质完全氧化最多可消耗9mol氧气
D.1mol该物质最多可与3molNaOH发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com