
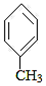
 +CO$→_{△}^{AlCl_{3},HCl}$
+CO$→_{△}^{AlCl_{3},HCl}$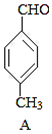 $→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$
$→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$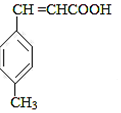 $→_{浓硫酸,△}^{CH_{3}OH}$E
$→_{浓硫酸,△}^{CH_{3}OH}$E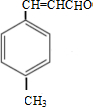 ,生成E的反应类型为酯化反应或取代反应
,生成E的反应类型为酯化反应或取代反应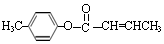 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为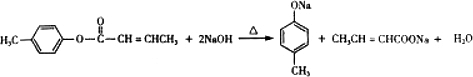 .
. .
. 分析 由合成路线可知,甲苯发生取代反应生成A对甲基苯甲醛,再与CH3CHO在碱性条件下反应生成B,B为 ,①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到
,①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到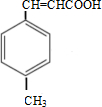 ,再与甲醇发生酯化反应生成E为
,再与甲醇发生酯化反应生成E为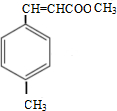 ,然后结合有机物的结构与性质来解答.
,然后结合有机物的结构与性质来解答.
解答 解:(1)A含-CHO,官能团的名称为醛基,A分子中含4种H,核磁共振氢谱各峰值比为1:2:2:3,
故答案为:醛基;1:2:2:3;
(2)物质B的结构简式为 ,生成E的反应类型为酯化反应或取代反应,
,生成E的反应类型为酯化反应或取代反应,
故答案为: ;酯化反应或取代反应;
;酯化反应或取代反应;
(3)试剂C可氧化-CHO,不能氧化碳碳双键,只有 b.银氨溶液、d.新制Cu(OH)2悬浊液符合,
故答案为:bd;
(4)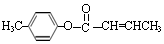 是E的一种同分异构体,E同分异构体中含-COOC-,与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,E同分异构体中含-COOC-,与足量NaOH溶液共热的化学方程式为 ,
,
故答案为: ;
;
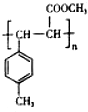
(5)遇FeCl3溶液显紫色,则含酚-OH,且苯环上有两个取代基,另一取代基为-CH=CH2,则符合条件的A的同分异构体为邻、间、对乙烯基苯酚3种,E中含C=C,在一定条件下可以生成高聚物F,发生加聚反应,则F的结构简式为 ,
,
故答案为:3; .
.
点评 本题考查有机物的合成,为高频考点,把握合成流程中官能团的变化、碳链变化、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题
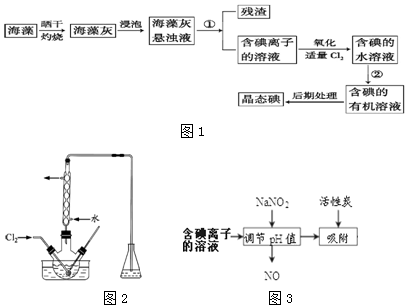
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
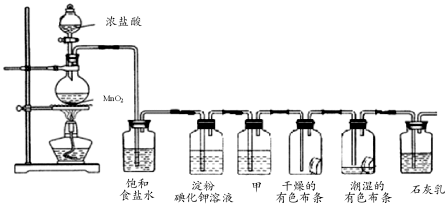
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 物质 | 起始浓度/(mol•L-1) | 平衡浓度/(mol•L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.0142 |
| NO2 | 0.100 | 0.0716 |
| A. | 平衡时,Ⅰ、Ⅱ中反应的转化率α(N2O4)>α(NO2) | |
| B. | 平衡后,升高相同温度,以N2O4表示的反应速率v(Ⅰ)<v(Ⅱ) | |
| C. | 平衡时,Ⅰ、Ⅱ中正反应的平衡常数K(Ⅰ)=$\frac{Ⅰ}{K(Ⅱ)}$ | |
| D. | 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
 CH3CO18OC2H5+H2O.
CH3CO18OC2H5+H2O.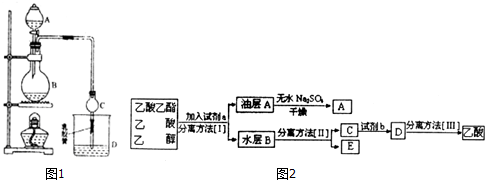
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com