
����Ŀ����ˮ���Ȼ���������ýȾ�����л��ϳ��е��Ȼ�������ʵ���ҿ������ڵ���![]() �۵�
�۵�![]() ��
��![]() ��Ӧ�Ʊ�
��Ӧ�Ʊ�![]() ��װ����ͼ��
��װ����ͼ��
��֪��![]() ��
��![]() �й��������ʣ�
�й��������ʣ�
���� | ��ɫ��״̬ | �۵�/�� | �е�/�� |
SnCl2 | ��ɫ���� | 246 | 652 |
SnCl4 | ��ɫҺ�� | -33 | 114 |
![]() ����ˮ������
����ˮ������![]() ���ش��������⣺
���ش��������⣺
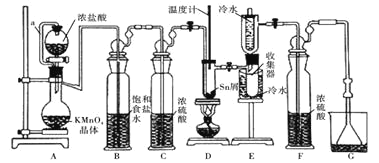
��1������a��������____________��װ��A�з�����Ӧ�����ӷ���ʽΪ____________________��
��2�����۲쵽װ��FҺ���Ϸ�___________ʱ�ſ�ʼ��ȼD���ľƾ��ƣ������ۻ����ʵ����������������������ȡ���ʱ�������ȵ�Ŀ����![]() ________��
________��![]() ______
______
��3��������װ����ȱ��װ��![]() ��������ͬ
��������ͬ![]() ����D����֧�Թ��з�������Ҫ����Ӧ��ѧ����ʽΪ_________________________________��
����D����֧�Թ��з�������Ҫ����Ӧ��ѧ����ʽΪ_________________________________��
��4��![]() �����ķ�Ӧ������
�����ķ�Ӧ��������
![]() ��Ϊ��ֹ��Ʒ�д�������
��Ϊ��ֹ��Ʒ�д�������![]() ���ɲ�ȡ�Ĵ�ʩ��____________________________________________��
���ɲ�ȡ�Ĵ�ʩ��____________________________________________��
��5���ζ�������Ʒ��2��![]() ��
��![]() �ĺ������÷�����ƽ��ȡ
�ĺ������÷�����ƽ��ȡ![]() ��Ʒ����ƿ�У�������ˮ�ܽ⣬���������Һ����
��Ʒ����ƿ�У�������ˮ�ܽ⣬���������Һ����![]() �ĵ����Һ�ζ����յ�ʱ����
�ĵ����Һ�ζ����յ�ʱ����![]() �����Ʒ��
�����Ʒ��![]() ��
��![]() ����������Ϊ___________��
����������Ϊ___________��![]() С�������2λ����֪
С�������2λ����֪![]()
���𰸡�ʹ��Һ©���ڵ�Һ��˳������ ![]() ���ֻ���ɫ���� �ӿ�����������Ӧ������ ʹ
���ֻ���ɫ���� �ӿ�����������Ӧ������ ʹ![]() ������������ӻ�����з������
������������ӻ�����з������ ![]() ����Sn�������ķ�Ӧ�¶���
����Sn�������ķ�Ӧ�¶���![]() ��
��![]() ֮�� ��ͨ���������
֮�� ��ͨ��������� ![]()
��������
![]() ����a��������ʹ��Һ©����Բ����ƿ��ѹǿ��ȣ�
����a��������ʹ��Һ©����Բ����ƿ��ѹǿ��ȣ�![]() �и��������Ũ���ᷢ����Ӧ�����Ȼ��ء��Ȼ��̡�������ˮ��
�и��������Ũ���ᷢ����Ӧ�����Ȼ��ء��Ȼ��̡�������ˮ��
![]() ��
��![]() ��Ӧǰ��Ҫ��������װ���еĿ����ž����¶�Խ�߷�Ӧ����Խ�졢���¿���ʹ
��Ӧǰ��Ҫ��������װ���еĿ����ž����¶�Խ�߷�Ӧ����Խ�졢���¿���ʹ![]() ������
������
![]() ������֪������֪
������֪������֪![]() ��ˮ������
��ˮ������![]() ��
��
![]() ������֪������ͨ������������������¶ȵ���
������֪������ͨ������������������¶ȵ���![]() �ķе����
�ķе����![]() �Ļӷ����ɷ�ֹ��Ʒ�д�������
�Ļӷ����ɷ�ֹ��Ʒ�д�������![]() ��
��
![]() ����
����![]() ����
����![]() ��
��![]() �����
�����
![]() ����a��������ʹ��Һ©����Բ����ƿ��ѹǿ��ȣ�����Һ��˳�����£����������Ũ���ᷴӦ�����ӷ���ʽΪ
����a��������ʹ��Һ©����Բ����ƿ��ѹǿ��ȣ�����Һ��˳�����£����������Ũ���ᷴӦ�����ӷ���ʽΪ![]() ��
��
![]() ��
��![]() ��Ӧǰ��Ҫ��װ���еĿ����ž�����F�п�������ɫ˵��װ���п������ž����������ȵ�Ŀ����
��Ӧǰ��Ҫ��װ���еĿ����ž�����F�п�������ɫ˵��װ���п������ž����������ȵ�Ŀ����![]() �����¶ȣ��ӿ�����������Ӧ�����ʣ�
�����¶ȣ��ӿ�����������Ӧ�����ʣ�![]() ����
����![]() ��
��![]() ���۷е��֪������ʹ
���۷е��֪������ʹ![]() ������������ӻ�����з����������������¶ȡ�
������������ӻ�����з����������������¶ȡ�
![]() ������֪����
������֪����![]() ����ˮ������
����ˮ������![]() �����Է�Ӧ����ʽ��
�����Է�Ӧ����ʽ��![]() ��
��
![]() ��֪�����Ϣ�����ڵ���
��֪�����Ϣ�����ڵ���![]() �۵�
�۵�![]() ��
��![]() ��Ӧ�Ʊ�
��Ӧ�Ʊ�![]() ��Ϊ��֤�����ڣ��¶������
��Ϊ��֤�����ڣ��¶������![]() ������
������![]() ��
��![]() ���۷е�ɵÿ��Ʒ�Ӧ�¶Ȳ��ܸ���
���۷е�ɵÿ��Ʒ�Ӧ�¶Ȳ��ܸ���![]() ��ͨ�������������
��ͨ�������������![]() �IJ������Է�ֹ��Ʒ�д�������
�IJ������Է�ֹ��Ʒ�д�������![]() ��
��
![]() �������ӷ���ʽ��
�������ӷ���ʽ��![]() ��
��![]() �����Ʒ��
�����Ʒ��![]() ��
��![]() ���
���![]() ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018��10��15�գ��й��á����������ҡ����ػ���ɹ��ԡ�һ��˫�ǡ���ʽ���䱱������ȫ����������ϵͳ��15��16�����ǣ������ƽ���Ϊ������泥�NH4ClO4���ȡ��Ʊ�NH4ClO4�Ĺ����������£�
����ʳ��ˮ![]() NaClO3
NaClO3![]() NaClO4
NaClO4![]() NaClO4
NaClO4![]() NH4ClO4
NH4ClO4
����˵���������
A. NH4ClO4�������ӻ�����
B. �ܽ�ȣ�NaClO4��NH4ClO4
C. ���NaClO3��Һʱ������ӦʽΪClO3-��H2O��2e-=C1O4-��2H+
D. �������п�ѭ�����õ�������NH4Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п�����̵���![]() ��Ҫ�ɷ�ΪZnO����������
��Ҫ�ɷ�ΪZnO����������![]() ��CuO��
��CuO��![]() ��MnO��
��MnO��![]() Ϊԭ�Ͽ���������п����ZnSO4��2H2O��Ħ������Ϊ189g/mol��
Ϊԭ�Ͽ���������п����ZnSO4��2H2O��Ħ������Ϊ189g/mol��
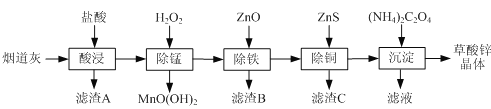
�й��������↑ʼ�����ͳ�����ȫ��pH���±���
�������� |
|
|
|
|
��ʼ������pH |
|
|
|
|
������ȫ��pH |
|
|
|
|
���ʴ��������⣺
(1)����A����Ҫ�ɷ�Ϊ_________������B����Ҫ�ɷ�Ϊ_______________��
(2)���̹����в���![]() ���������ӷ���ʽΪ_______________________��
���������ӷ���ʽΪ_______________________��
(3) �ٳ���![]() ����
����![]() ���ܱ���ȥ
���ܱ���ȥ![]() ʱ����ZnO���Ʒ�ӦҺpH�ķ�ΧΪ______________��
ʱ����ZnO���Ʒ�ӦҺpH�ķ�ΧΪ______________��
����ij��Һ�к���![]() �����ܺ���
�����ܺ���![]() �������ʵ��֤��
�������ʵ��֤��![]() �Ĵ��ڡ�________��
�Ĵ��ڡ�________��
(4)������Ҫ��ø��﴿������п���壬����еIJ�����_______________��
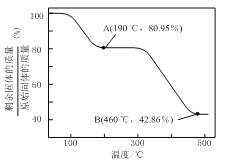
(5)������п������ȷֽ�ɵõ�һ�����ײ��ϡ����ȹ����й�����������¶ȵı仯��ͼ��ʾ��![]() ��Χ�ڣ�������Ӧ�Ļ�ѧ����ʽΪ_________________��
��Χ�ڣ�������Ӧ�Ļ�ѧ����ʽΪ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͬ������ͭ�ֱ����Ũ���ᡢϡ���ᷴӦ������������ȷ����
A. ��Ӧ���ҳ̶ȣ�������ͬ
B. ������������ʵ�����ǰ�߶࣬������
C. ��Ӧ�����������ɫ��ǰ��dz��������
D. ��Ӧ��ת�Ƶĵ���������ǰ�߶࣬������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д�����з�Ӧ�Ļ�ѧ����ʽ����ע��(1)��(2)��(3)�ķ�Ӧ����
(1)����ϩ�Ʊ�����ϩ�ķ�Ӧ _______________��Ӧ���ͣ�_________________
(2)�üױ���TNT�ķ�Ӧ __________________��Ӧ���ͣ�_________________
(3)��������NaOH���Ҵ���Һ���� _________________��Ӧ���ͣ�_____________
(4)ϩ����һ������������ʱ������C=C�����ѣ�ת��Ϊȩ��ͪ���磺![]() ����
����![]() ���������������·�����Ӧ����д����Ӧ�ķ���ʽ _________________________ ��
���������������·�����Ӧ����д����Ӧ�ķ���ʽ _________________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����d����е����Ų���![]() �������Ų���
�������Ų���![]() ����ֱ�ӵĸ�����
����ֱ�ӵĸ�����
A.�������ԭ��B.����������ԭ��C.�ӻ��������D.���ع���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ��Ӧ 2H2(g)��O2(g)=2H2O(g)�������仯ʾ��ͼ�� ����˵����ȷ����
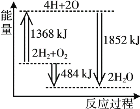
A.�� 2 mol H2(g)�� 1 mol O2(g)�еĻ�ѧ����ΪH��Oԭ�ӣ����ų�1368 kJ ����
B.�� H��O ԭ���γ� 2 mol H2O(g)��������1852 kJ ����
C.2 mol H2(g)�� 1 mol O2(g)��Ӧ���� 2 mol H2O(g)�����ų�484 kJ ����
D.2 mol H2(g)�� 1 mol O2(g)��Ӧ���� 2 mol H2O(l)����H����484 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ij��̼�Ͻ𣨿ɿ�������̼���ֵ��ʵĻ�����ij��ѧ��ȤС��Ϊ�˲ⶨ��̼�Ͻ���̼�������������������ͼ��ʾ��ʵ��װ�ã��г�������ʡ�ԣ���
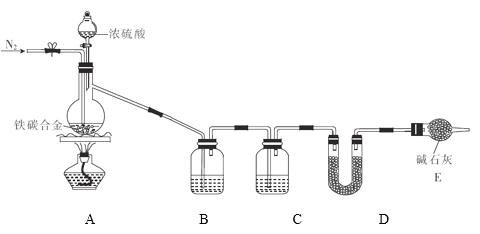
(1)װ��A�з����ķ�Ӧ����![]() ������________________��
������________________��
(2)����������
װ�ô��� | B | C | D |
��ʢ�Լ� | ���� | ��________ | ��____________ |
װ������ | ��_____________ | �������� | ��___________ |
(3)����̼�Ͻ������Ϊ5.00g����ַ�Ӧ��Ƶ�Dװ������0.66g����Ͻ���̼����������Ϊ_______����ȱ��Eװ�ã�������̼����������_________������ƫ������ƫ����������Ӱ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������β�������е�һ����Ӧ���£�2NO(g)+2CO(g)N2(g)+2CO2(g)����ش��������⣺
(1)��֪��N2(g)+O2(g)=2NO(g)��H=+180.5kJ��mol-l
C(s)+O2(g)=CO2(g) ��H=-393.5kJ��mol-l
2C(s)+O2(g)=2CO(g) ��H=-221kJ��mol-l
��2NO(g)+2CO(g)N2(g)+2CO2(g)����H=____kJ��mol-l��
(2)һ���¶��£������Ϊ 1 L���ܱ������г���һ������NO��CO����t1ʱ�̴ﵽƽ��״̬����ʱn(CO)=0.1 mol��n(NO)=0.2 mol��n(N2)= a mol����N2ռƽ���������![]() ��
��
����÷�Ӧ��ƽ�ⳣ��K=______���������¶ȼ�����������䣬ƽ����ڴ˻��������������г���3a mol��N2��0.2 mol��NO��ƽ�⽫______�ƶ�(����������������������������)��
�����и����������˵���÷�Ӧ�Ѿ��ﵽƽ�����______��
A��v����(CO2)= v����(CO)
B�����������ܶȲ��ٸı�
C����������ƽ����Է����������ٸı�
D��NO��CO��N2��CO2��Ũ�Ⱦ����ٱ仯
E����λʱ��������2n mol̼��˫����ͬʱ����n molN��N
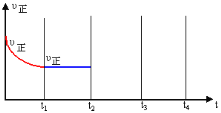
����t2ʱ�̣�������Ѹ��ѹ����ԭ�ݻ���![]() ���������������������£� t3ʱ�̴ﵽ�µ�ƽ��״̬������ͼ�в��仭��t2��t3��t4ʱ�Σ�����Ӧ���ʵı仯����_________��
���������������������£� t3ʱ�̴ﵽ�µ�ƽ��״̬������ͼ�в��仭��t2��t3��t4ʱ�Σ�����Ӧ���ʵı仯����_________��
(3)Ϊ��������β���е��к�����Դ�������Ⱦ����������װβ������װ�á�����װ����װ�к�Pd�ȹ���Ԫ�صĴ����������ڴ�������������������õĻ�������ͼ��ʾ��д�������仯�е��ܻ�ѧ��Ӧ����ʽ_________��

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com