
����Ŀ������Ȼ�����У�һ����ʹ�õľ۱���ϩ���ϴ����ġ���ɫ��Ⱦ����Ϊͻ�������ֲ������Էֽ⣬�����鷳��������Ƴ�һ�����͵IJ����ܴ���۱���ϩ���������������۶����ɵģ����ֲ��Ͽ�������������½��⡣���й��ھ�����(�ṹ��ʽΪ )��˵����ȷ����
)��˵����ȷ����
A.��������һ�ִ�����
B.��ۺϷ�ʽ�뱽��ϩ����
C.�䵥��Ϊ CH3��CH2��COOH
D.��������һ�����߷��Ӳ���
���𰸡�D
��������
A.�Ӿ�����ṹ��֪���������Ǹ߷��ӻ���������߷��ӻ������е�nֵ����������Ϊ������A����
B.���ݾ�����Ľṹ��֪���������������е��ǻ����Ȼ���ˮ�IJ������������۷�Ӧ���۱���ϩ���ɵ���![]() �е�̼̼˫���Ӿ۶��ɣ���B����
�е�̼̼˫���Ӿ۶��ɣ���B����
C. Ϊ������ĵ��壬��C����
Ϊ������ĵ��壬��C����
D.�����������ǻ����Ȼ��������ɵĸ߷��ӻ���������һ�����߷��Ӳ������������߷��ӵ����ʣ���D��ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T��ʱ����ij�����ܱ������г���![]() ��
��![]() ������Ӧ��
������Ӧ��![]() ����Ӧ�����������ı仯��ͼ��ʾ������˵��������� ( )
����Ӧ�����������ı仯��ͼ��ʾ������˵��������� ( )
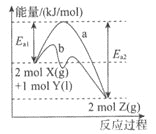
A.Y����������ʱ���÷�Ӧ�ﵽƽ��״̬
B.��Ӧ�ﵽƽ��ʱ���ų�������С��![]()
C.����bΪ�������ʱ�÷�Ӧ�ķ�Ӧ����ͼ
D.�����������䣬ƽ����ٳ���![]() ���ﵽ��ƽ��ʱ��Z�����������С
���ﵽ��ƽ��ʱ��Z�����������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�����ʵ�����ӷ���ʽ����ȷ����
A.��ʯī�缫��ⱥ��ʳ��ˮ��2Cl-+2H2O![]() 2OH-+H2��+Cl2��
2OH-+H2��+Cl2��
B.������������ˮ����Al3++3H2O��Al(OH)3��+3H+
C.�����������ϵ��ͭ�������ĵ缫��ӦΪ��Cu2+��2e-=Cu
D.��������þ��Һ�е����̪��Һ����Һ��죺Mg(OH)2(s)Mg2+(aq)+2OH-(aq)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����()
![]() ���ӻ����ﺬ���Ӽ���Ҳ���ܺ����Լ���Ǽ��Լ�
���ӻ����ﺬ���Ӽ���Ҳ���ܺ����Լ���Ǽ��Լ�
![]() ��������Դ���̼������ԣ����Էǽ�����
��������Դ���̼������ԣ����Էǽ�����![]()
![]() ������Ԫ�صĻ����ﲻһ�������ӻ�����
������Ԫ�صĻ����ﲻһ�������ӻ�����
![]() �ɷǽ���Ԫ����ɵĻ�����һ���ǹ��ۻ�����
�ɷǽ���Ԫ����ɵĻ�����һ���ǹ��ۻ�����
![]() ����״̬�ܵ���Ļ����������ӻ�����
����״̬�ܵ���Ļ����������ӻ�����
![]() �ɷ�����ɵ�������һ�����ڹ��ۼ�
�ɷ�����ɵ�������һ�����ڹ��ۼ�
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�ӦA(g)+4B(g)![]() 2C(g)+2D(g)���������ݱ�ʾ��Ӧ���е������ǣ� ��
2C(g)+2D(g)���������ݱ�ʾ��Ӧ���е������ǣ� ��
A.v(A)=1.4mol/(Ls)B.v(B)=3.6 mol/(Ls)
C.v(C)=2mol/(Ls)D.v(D)=30 mol/(Lmin)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ������˵������ȷ���ǣ� ��
A. ij�¶��£�Ba(OH)2��Һ��Kw=10-12,��pH=8�ĸ���Һ�м�������pH=4�����ᣬ��ַ�Ӧ�����Һ��pH=6
B. ˮ���������c(H+)=10-13mol/L����Һ��K+��Cl-��NO3-��I-���ܴ�������
C. ��0.1mol/LNH4Cl��Һ�в��ϼ���NaOH����,����NaOH�ļ��룬![]() ���ϼ�С
���ϼ�С
D. һ���¶��£��������ƴﵽ�ܽ�ƽ�⣬�����Һ�м������������Ʒ�ĩ(��������ЧӦ),����Һ��c(Ca2+)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���۲��±�ģ�Ͳ�����й���Ϣ���ж�����˵���в���ȷ����( )
B12�ṹ��Ԫ | SF6���� | S8���� | HCN | |
�ṹģ��ʾ��ͼ |
|
|
|
|
��ע | �۵�1873 K | �� | ������CS2 | �� |
A.����������ԭ�Ӿ��壬ÿ��B12�ṹ��Ԫ�к���30��B��B����20����������
B.SF6���ɼ��Լ����ɵķǼ��Է���
C.��̬��S8����ԭ�Ӿ���
D.HCN�ĽṹʽΪH��C��N
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ͼ��1mol NO2(g)��1mol CO(g)��Ӧ����CO2��NO�����е������仯ʾ��ͼ����֪E1��+134kJ��mol��1��E2��+368kJ��mol��1�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯��________(��������������С����������������ͬ)����H�ı仯��________����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ��________��
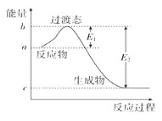
��2����CO2��NH3Ϊԭ�Ͽɺϳɻ�������[��ѧʽΪCO(NH2)2]����֪��
a��2NH3(g)+CO2(g)=NH2CO2NH4(s) ��H����159.5kJ��mol��1
b��NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ��H��+116.5kJ��mol��1
c��H2O(l)=H2O(g) ��H��+44.0kJ��mol��1
д��CO2��NH3�ϳ����غ�Һ̬ˮ���Ȼ�ѧ��Ӧ����ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����пƬ��ͭƬ����ͬ��ʽ����ϡ�����У�����˵����ȷ���ǣ� ��

A. ���е��Ӿ����ߴ�ͭƬ����пƬ
B. ���ձ���пƬ�Ͼ�������ԭ��Ӧ
C. ���ձ���ͭƬ����������ݲ���
D. һ��ʱ������ձ�����Һ��c��H+������С
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com