
| A. | 32g硫 | B. | 64g Cu2+ | ||
| C. | 32g氧气 | D. | 6.02×1024个水分子 |
分析 根据n=$\frac{m}{M}$计算硫、Cu2+、氧气物质的量,根据n=$\frac{N}{{N}_{A}}$计算水的物质的量.
解答 解:32g硫的物质的量为$\frac{32g}{32g/mol}$=1mol,
64Cu2+的物质的量为$\frac{64g}{64g/mol}$=1mol,
32g氧气物质的量为$\frac{32g}{32g/mol}$=1mol,
6.02×1024个水分子的物质的量为$\frac{6.02×1{0}^{24}}{6.02×1{0}^{23}mo{l}^{-1}}$=10mol,
故选:D.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的有关计算.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
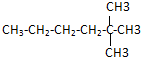 用“键线式”可表示为
用“键线式”可表示为 ,其中每个端点和转折点都表示一个碳原子,氢原子已省略.某有机物分子用键线式表示为
,其中每个端点和转折点都表示一个碳原子,氢原子已省略.某有机物分子用键线式表示为 ,该有机物的分子式为:C10H20,其一氯代物有4种.
,该有机物的分子式为:C10H20,其一氯代物有4种.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
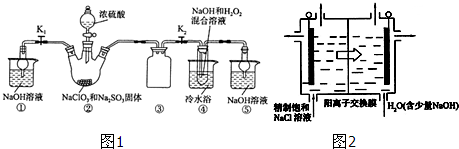
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com