
【题目】水溶液中能大量共存的一组离子是( )
A.NH4+、Ba2+、Br﹣、CO32﹣
B.Cl﹣、SO32﹣、Fe2+、H+
C.K+、Na+、SO42﹣、MnO4﹣
D.Na+、H+、NO3﹣、HCO3﹣
科目:高中化学 来源: 题型:
【题目】在NaCN溶液中存在水解平衡:CN-+H2O![]() HCN+OH-,水解常数
HCN+OH-,水解常数![]() [co(NaCN)是NaCN溶液的起始浓度]。25℃向1mol/L的NaCN溶液中不断加水稀释,NaCN溶液浓度的对数值lgc0与2pOH[p0H=-lgc(0H-)]的关系下图所示,下列说法错误的是
[co(NaCN)是NaCN溶液的起始浓度]。25℃向1mol/L的NaCN溶液中不断加水稀释,NaCN溶液浓度的对数值lgc0与2pOH[p0H=-lgc(0H-)]的关系下图所示,下列说法错误的是
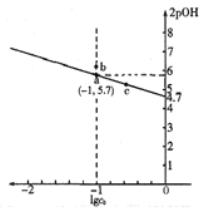
A. 25℃时,Kn(CN-)的值为10-4.7
B. 升高温度,可使曲线上a点变到b点
C. 25℃,向a点对应的溶液中加入固体NaCN,CN-的水解程度减小
D. c点对应溶液中的c(OH-)大于a点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学反应原理研究碳、硫及其化合物的性质具有重要意义。
(1)工业上用炭还原辉铜矿(主要成分是Cu2S),可制取金属铜。
己知反应的热化学方程式如下:
C(s)+S2(g)=CS2(g) △H1=150kJ/mol
Cu2S(s)+H2(g)=2Cu(s)+H2S(g) △H2=59.5kJ/mol
2H2S(g)=2H2(g)+S2(g) △H3=170kJ/mol
通过计算,可知用炭还原Cu2S制取金属铜和CS2(g)的热化学方程式为_________。
(2)为研究反应2H2S(g)![]() 2H2(g)+S2(g)对上述工业过程的影响,兴趣小组进行如下探究:
2H2(g)+S2(g)对上述工业过程的影响,兴趣小组进行如下探究:
①向三个体积均为1L的恒容密闭容器中分别加入1molH2S,进行H2S分解实验。不同温度下测得H2S的转化率与时间的关系如下图所示:
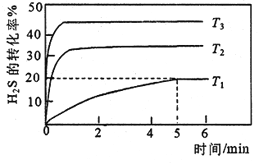
T1温度下,0~5minS2(g)的平均反应速率v(S2)= _____mol.L-1.min-1,反应平衡常数K=_____mol.L-1。温度T1、T2、T3由高到低的顺序是________。
②T4温度时,向1L的恒容密闭容器中加入1.8molH2(g)、1.2molS2(g),达到平衡后测得S2(g)和H2S(g)的浓度相等,则T4______T1(填“<”、“=”或“>”)。
(3)T℃时,向某浓度的草酸溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中三种微粒H2C2O4、HC2O4-、C2O42-的物质的量分数(δ)与pH的关系如下图所示:

①草酸的电离常数分别为K1与K2,则![]() =______。
=______。
②按投料比n(Na2C2O4):n(NaHC2O4)=2:1配成溶液,下列有关该溶液的叙述正确的是____(填序号)。
A. 该溶液的pH为4.2
B. 3c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-)
C. 3c(Na+)=5[c(HC2O4-)+c(C2O42-)+c(H2C2O4)]
D. 3c(OH-)+c(C2O42-)=3c(H+)+2c(HC2O4-)+5c(H2C2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的性质比较:①酸性:HClO4>H2SO4>H3PO4 ②最高正化合价:Cl>N>C ③稳定性:HCl>HBr>HI ④还原性:HCl>HBr正确的是
A.①②③B.②③④C.①②④D.全部都正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是
A. 常温常压下,11.2LO3所含的原子数为1.5NA
B. 常温常压下,18gH2O所含的分子数为NA
C. 标准状况下,16gO2所含的原子数为6NA
D. 标准状况下,11.2L氢气和氦气的混合气体所含的原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知几种难溶电解质的溶度积如下表所示:
几种难溶电解质的Ksp(25℃) | |
沉淀溶解平衡 | Ksp |
AgBr(s) | 5,0×10-13 mol2·L-2 |
AgI(s) | 8.3×10-17 mol2·L-2 |
FeS(s) | 6.3×10-18 mol2·L-2 |
ZnS(s) | 1.6×10-24 mol2·L-2 |
CuS(s) | 1.3×10-36 mol2·L-2 |
(1)AgBr、AgI、FeS、ZnS、CuS的溶解能力由大到小的顺为:____________________。
(2)向饱和的AgI溶液中加入固体硝酸银,则c( I- )________(填“增大”、“减小”或“不变”),若改加AgBr固体,则c(Ag+)__________(填“增大”、“减小”或“不变”)。
(3)在25℃时,向100mL浓度均为0.1 mol·L-1 FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是_____________________(用沉淀物的化学式表示)。
(4)在25℃时,把ZnS加入蒸馏水中,一定时间后达到如下平衡: ZnS(s)![]() Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是 _______。
Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是 _______。
A.加入少量CuS固体 B.加入少量FeS固体
C.加入少量FeCl2固体 D.加入少量CuCl2固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com