
| A、碳酸氢钠的热稳定性小于碳酸钠的 |
| B、Fe在足量Cl2中燃烧生成FeCl2和FeCl3 |
| C、可用石灰水区分Na2CO3与NaHCO3溶液 |
| D、滴加石蕊试液显红色的溶液:Fe3+、NH4+、I-可能大量共存 |
| ||


科目:高中化学 来源: 题型:
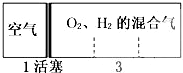
| A、①② | B、②④ | C、③④ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠、铝均能从FeCl3溶液中置换出铁单质 |
| B、均能与盐酸反应,但金属钠与盐酸的反应最剧烈 |
| C、在地壳中的含量:Al>Fe>Na |
| D、钠、铝均能与NaOH溶液反应,但参加反应的物质种类前者少于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应速率关系是:2v正(A)=3v正(D) |
| B、若单位时间内生成x mol C的同时,消耗x mol A,则反应一定处于平衡状态 |
| C、达到化学平衡后,增大容器的容积,则正反应速率减小,逆反应速率增大 |
| D、达到化学平衡后,升高温度,则C的质量分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
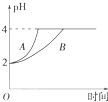 请回答下列问题:
请回答下列问题:| 温度/℃ | 800 | 1 000 | 1 200 | 1 400 |
| 平衡常数 | 0.45 | 1.92 | 276.5 | 1 771.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com