
| A. | 甲醛 | B. | 3-甲基丁醛 | C. | 已醛 | D. | 丁醛 |
分析 饱和一元醛的通式是CnH2nO,根据醛基和银的关系-CHO~2Ag(甲醛为-CHO~4Ag),结合生成金属银的量可以获得醛的物质的量,根据生成二氧化碳的量结合碳原子守恒可以获得C的个数,进而确定分子式即可.
解答 解:生成银的物质的量为:n(Ag)=$\frac{21.6g}{108g/mol}$=0.2mol,点燃生成CO2的物质的量n(CO2)=$\frac{8.96L}{22.4L/mol}$=0.4mol,
若为甲醛,醛基和银的关系-CHO~4Ag,则甲醛的物质的量为:$\frac{0.2mol}{4}$=0.05mol,甲醛中含有碳原子数为:$\frac{0.4mol}{0.05mol}$=8,不满足条件;
若其它饱和一元醛,醛基和银的关系-CHO~2Ag,所以n(-CHO)=0.1mol,即饱和一元醛的物质的量为0.1mol,含有碳原子数目为4,分子式为:C4H8O,为丁醛,
故选D.
点评 本题考查有机物分子式确定的计算,题目难度不大,涉及醛的银镜反应,解题关键抓住-CHO~2Ag关系确定醛的物质的量,注意甲醛与Ag的物质的量之比为1:4,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 升高温度 | B. | 降低温度 | C. | 使用催化剂 | D. | 增大反应物浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验事实 | 结论或原因 | |
| A | SO2的水溶液可以导电 | SO2是电解质 |
| B | 漂白粉在空气中久置变质 | 漂白粉中的Ca(ClO)2与空气中的CO2反应生成CaCO3和见光易分解的HClO |
| C | 石灰石与二氧化硅在高温下反应可制得硅酸钙 | 非金属性:Si>C |
| D | 碳酸氢钠可用作食品的膨松剂 | 碳酸氢钠能与碱反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.77×10-4 | 4.9×10-16 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 2CN-+H2O+CO2═2HCN+CO32- | |
| B. | 2HCOOH+CO32-═2HCOO-+H2O+CO2↑ | |
| C. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 | |
| D. | HCOOH+CN-═HCOO-+HCN |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
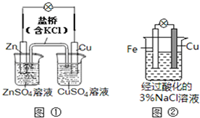
| A. | 图①中正极附近溶液pH降低 | |
| B. | 图①中电子由Zn流向Cu,盐桥中的Cl-移向CuSO4溶液 | |
| C. | 图②中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成 | |
| D. | 图②正极反应是O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向沸水中滴加饱和氯化铁溶液制备胶体,用可见光束照射,产生丁达尔效应 | |
| B. | 常温下,向0.10mol•L-1NaHCO3溶液,滴加CaCl2溶液至pH=7,滴加过程中产生白色沉淀,但无气体放出,说明加入CaCl2促进了HCO3-的水解 | |
| C. | 利用以下实验器材(规格数量不限):烧杯、量筒、环形玻璃搅拌棒、纸条、硬纸板、温度计能完成中和反应反应热的测定 | |
| D. | 向浓度均为0.1mol•L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水,先出现蓝色沉淀,因为KSP[Mg(OH)2]>KSP[Cu(OH)2] |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
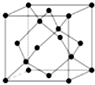 A、B、C、D、E、F为原子序数依次增大的六种元素,A的一种同位素可用于考古测定生物的死亡年代,C原子的最外层电子数是次外层的3倍,D与B同主族;E的原子序数是A、B之和的2倍;F的原子序数为29.回答下列问题:
A、B、C、D、E、F为原子序数依次增大的六种元素,A的一种同位素可用于考古测定生物的死亡年代,C原子的最外层电子数是次外层的3倍,D与B同主族;E的原子序数是A、B之和的2倍;F的原子序数为29.回答下列问题: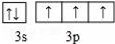 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,4.48LCHCl3的分子数为0.2 NA | |
| B. | 常温常压下,8gCH4含有5NA个电子 | |
| C. | 6.0g冰醋酸与4.6g乙醇反应生成乙酸乙酯的分子数为0.1 NA | |
| D. | 28 g由C2H4和C3H6组成的混合物中含有氢原子的数目为4 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com