
【题目】某种![]() 工程树脂由丙烯腈(
工程树脂由丙烯腈(![]() ,用
,用![]() 表示)、1,
表示)、1,![]() 丁二烯(
丁二烯(![]() ,用
,用![]() 表示)和苯乙烯(
表示)和苯乙烯(![]() ,用
,用![]() 表示)按一定比例共聚而得。
表示)按一定比例共聚而得。
(1)![]() 和
和![]() 三种单体中,
三种单体中,![]() 原子个数比的比值最小的单体是___________(填物质名称)。
原子个数比的比值最小的单体是___________(填物质名称)。
(2)经元素分析可知,该![]() 工程树脂的组成为
工程树脂的组成为![]() (
(![]() 为正整数),则原料中
为正整数),则原料中![]() 和
和![]() 的物质的量之比是____________(用
的物质的量之比是____________(用![]() 表示)。
表示)。
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g) △H<0,下列研究目的和示意图相符的是( )
2NH3(g) △H<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响 (p2>p1) | 温度对反应的影响 | 平衡体系中增加N2的浓度对反应的影响 | 催化剂对反应的影响 |
示意图 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配位键是一种特殊的化学键,其中共用电子对由某原子单方面提供。如![]() 就是由
就是由![]() (氮原子提供共用电子对)和
(氮原子提供共用电子对)和![]() (缺电子)通过配位键形成的。据此回答下列问题。
(缺电子)通过配位键形成的。据此回答下列问题。
(1)下列粒子中存在配位键的是__________(填序号)
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(2)硼酸(![]() )溶液呈酸性,试写出其电离方程式:____________________。
)溶液呈酸性,试写出其电离方程式:____________________。
(3)科学家对![]() 结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:
结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:
甲: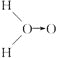 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
乙:HOOH
化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)________________。
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由人体尿液分离出来的结晶化合物A,熔点为187~188℃。现对化合物A进行如下实验:
(1)A的蒸气密度为8.0 g/L (已折合成标准状况)。取17.90 g A完全燃烧,将生成的气体先通过浓硫酸,浓硫酸质量增加8.10 g,再将剩余气体通过碱石灰,气体质量减轻39.60 g;另取17.90 g A使其完全分解,可得到1.12 L (标准状况)氮气。则A的分子式为_________________。
(2)A和足量6 mol/L的盐酸混合加热可以完全水解,1 mol A水解可生成1 mol B和1 mol C。已知:A、B、C三种物质的分子中均含有一个羧基;B仅由碳、氢、氧三种元素组成,三种元素原子的物质的量之比为7∶6∶2;C的名称为甘氨酸。试写出A的结构简式:_____________,B的分子式:_________,C的一种同分异构体的结构简式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T1时,在三个容积均为1 L的恒容密闭容器中仅发生反应 2NO2(g)2NO(g)+O2(g) ΔH>0。实验测得:υ正=υ(NO2)消耗=k正c2(NO2),υ逆=υ(NO)消耗=2υ(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是( )
容器编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A.反应达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为1∶1
B.反应达平衡时,容器Ⅱ中![]() 比容器Ⅰ中的大
比容器Ⅰ中的大
C.反应达平衡时,容器Ⅲ中NO的体积分数大于50%
D.当温度改变为T2时,若k正=k逆,则T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)若1mol有机物A能与1mol氢气发生加成反应,其加成产物是2,2,3-三甲基戊烷,则此有机物A可能的结构简式有___________。
(2)若1mol有机物A与2molH2发生加成反应,其加成产物为2,2,3-三甲基戊烷,则此有机物A可能的结构简式为______(注意:![]() 不稳定)。
不稳定)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的ΔH_____0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如图所示。在 0~60 s 时段, 反应速率 v(N2O4)为_____mol·L-1·s-1;反应的平衡转化率为:_____; 反应的平衡常数K1为_____。
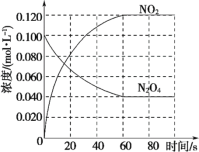
(2)100℃时达平衡后,改变反应温度为 T,N2O4以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
a:T____________100℃(填“大于”或“小于”),判断理由是__________。
b:计算温度T时反应的平衡常数K2____________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半。平衡向____________(填“正反应”或“逆反应”)方向移动,判断理由________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物Targretin(F)能治疗顽固性皮肤T细胞淋巴瘤,其合成路线如图所示:
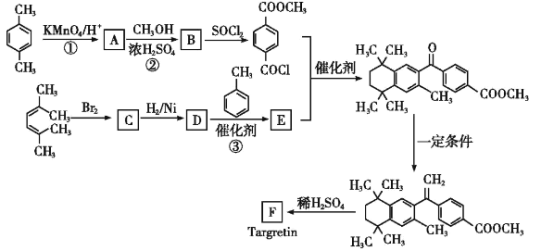
已知:
ⅰ.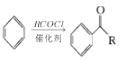
ⅱ.![]()
ⅲ.RCOOH![]() RCOCl(R表示烃基)
RCOCl(R表示烃基)
(1)反应①的反应类型是__。
(2)反应②的化学方程式:__。
(3)C的核磁共振氢谱图中有__个峰。
(4)反应③的化学方程式:__。
(5)F的分子式是C24H28O2。F中含有的官能团:__。
(6)写出满足下列条件A的两种同分异构体的结构简式(不考虑-O-O-或![]() 结构):__。
结构):__。
a.苯环上的一氯代物有两种
b.既能发生银镜反应又能发生水解反应
(7)已知:![]() (R、R′为烃基)。以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成
(R、R′为烃基)。以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成![]() ,写出合成路线__(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件。
,写出合成路线__(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池是化学电源的雏形。关于如图所示原电池的说法正确的是
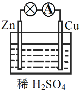
(1)如图连接好装置后,负极材料是__(填“Zn”或“Cu”),铜电极发生的现象:_____。
(2)相应原电池的总反应方程式为____。
(3)下列化学反应可通过原电池装置,可实现化学能直接转化为电能的是__(填序号)
①2NaOH+H2SO4=Na2SO4+2H2O
②Cu+2Fe3+=Cu2++2Fe2+
③C2H5OH+3O2![]() 2CO2+3H2O
2CO2+3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com