
| A. | 126C、136C、146C三种核素互为同素异形体 | |
| B. | 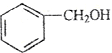 和 和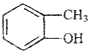 的分子式相同,化学性质也相同 的分子式相同,化学性质也相同 | |
| C. | 等质量的甲烷按a,b两种途径完全转化,途径a比途径b消耗更多的O2 途径a:CH$→_{催化剂}^{H_{2}O}$CO+H2$→_{燃烧}^{O_{2}}$CO2+H2O;途径b:CH4$→_{燃烧}^{O_{2}}$CO2+H2O | |
| D. | 铝热反应实验说明:在一定条件下铝的还原性强于很多难熔金属 |
分析 A.同素异形体是指同种元素组成的不同单质;
B.苯甲醇和邻甲基苯酚是不同类别的物质,官能团不同性质不同;
C.化学反应的热效应只与反应物的初始状态和生成物的最终状态有关;
D.铝热反应发生的依据是铝和金属氧化物发生的置换反应,铝的还原性强于难熔金属;
解答 解:A.126C、136C、146C三种核素是原子,互称为同位素,不是单质不能互为同素异形体,故A错误;
B.苯甲醇和邻甲基苯酚是不同类别的物质,分子式相同,官能团不同,属于同分异构体,性质不同,故B错误;
C.化学反应的热效应只与反应物的初始状态和生成物的最终状态有关,故ab两种途径,放出的热量一样多,耗氧量相同,故C错误;
D.铝可以和比铝金属性弱的金属氧化物发生铝热反应,铝热反应实验说明:在一定条件下铝的还原性强于很多难熔金属,故D正确;
故选D.
点评 本题考查了同素异形体、同位素、同分异构体、铝热反应原理等知识点,掌握基础是解题关键,题目难度不大.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正戊烷、新戊烷、异戊烷互为同分异构体 | |
| B. | 扁桃酸( )属于甲酸酯且有羟基直接连在苯环上的同分异构体共有13种 )属于甲酸酯且有羟基直接连在苯环上的同分异构体共有13种 | |
| C. |  互为同系物 互为同系物 | |
| D. | 四氯乙烯分子中所有原子都处于同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 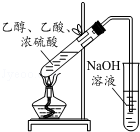 实验室中制取少量的乙酸乙酯 | |
| B. | 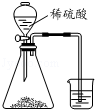 比较硫、碳、硅三种元素的非金属性强弱 | |
| C. | 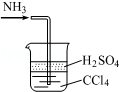 处理尾气 | |
| D. | 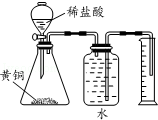 测定黄铜(Cu、Zn合金)中Zn 的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、B、C最简单氢化物的沸点依次递减,是因为A、B、C非金属性依次递减 | |
| B. | EB晶体是一种坚硬的高熔点材料,熔化时需克服离子键 | |
| C. | 在一定条件下,B的氧化物与B的简单氢化物均能反应生成单质B | |
| D. | C、D的常见氧化物均能溶于氢氧化钠溶液中,则C、D的氧化物均属于酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该温度下,加入NaHSO4可能引起由b向a的变化 | |
| B. | 该温度下,pH=2的盐酸与pH=12的氢氧化钠溶液等体积混合,所得溶液显中性 | |
| C. | 该温度下,加入Na2CO3溶液能引起b向c的变化 | |
| D. | 降低温度可能引起b向d的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 验证淀粉已水解 | 在淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的银氨溶液并水浴加热 |
| B | 比较醋酸和次氯酸的酸性强弱 | 用PH试纸测定0.1mol•L-1醋酸钠溶液和0.01mol•L-1次氯酸钠溶液的PH |
| C | 证明Cl2的氧化性比Br2氧化性强 | 0.1mol•L-1 NaBr溶液中加入适量的新制氯水,反应后再加入适量的四氯化碳,振荡,观察下层液体的颜色 |
| D | 除去苯中混有的少量苯酚 | 向其中加入适量的溴水再过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用量筒量取30mL溶液 | B. | 用四氯化碳萃取碘水中的碘 | ||
| C. | 用托盘天平称取2.5g固体 | D. | 用温度计代替玻璃棒搅拌溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
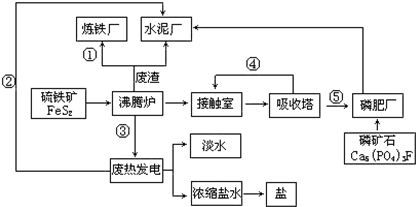
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com