
ÄÜÕżČ·±ķŹ¾ĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£Ø£©
A£® ÅØŃĪĖįÓėĢśŠ¼·“Ó¦£ŗ2Fe+6H+═2Fe3++3H2”ü
B£® ÄĘÓėCuSO4ČÜŅŗ·“Ó¦£ŗ2Na+Cu2+═Cu”ż+2Na+
C£® NaHCO3ČÜŅŗÓėĻ”H2SO4·“Ó¦£ŗCO32﹣+2H+═H2O+CO2”ü
D£® ĻņFeCl3ČÜŅŗÖŠ¼ÓČėMg£ØOH£©2£ŗ3Mg£ØOH£©2+2Fe3+═2Fe£ØOH£©3+3Mg2+
æ¼µć£ŗ Ąė×Ó·½³ĢŹ½µÄŹéŠ“£®
×ØĢā£ŗ Ąė×Ó·“Ó¦×ØĢā£®
·ÖĪö£ŗ A£®·“Ӧɜ³ÉĀČ»ÆŃĒĢśŗĶĒāĘų£»
B£®²»ÄÜÖĆ»»³öCu£¬·“Ӧɜ³ÉĒāŃõ»ÆĶ”¢ĮņĖįÄĘ”¢ĒāĘų£»
C£®HCO3﹣²»Äܲš·Ö£»
D£®·¢Éś³ĮµķµÄ×Ŗ»Æ£¬Éś³ÉĒāŃõ»ÆĢśŗĶĀČ»ÆĆ¾£®
½ā“š£ŗ ½ā£ŗA£®ÅØŃĪĖįÓėĢśŠ¼·“Ó¦µÄĄė×Ó·“Ó¦ĪŖFe+2H+═Fe2++H2”ü£¬¹ŹA“ķĪó£»
B£®ÄĘÓėCuSO4ČÜŅŗ·“Ó¦µÄĄė×Ó·“Ó¦ĪŖ2Na+2H2O+Cu2+═Cu£ØOH£©2”ż+2Na++H2”ü£¬¹ŹB“ķĪó£»
C£®NaHCO3ČÜŅŗÓėĻ”H2SO4·“Ó¦µÄĄė×Ó·“Ó¦ĪŖHCO3﹣+H+═H2O+CO2”ü£¬¹ŹC“ķĪó£»
D£®ĻņFeCl3ČÜŅŗÖŠ¼ÓČėMg£ØOH£©2µÄĄė×Ó·“Ó¦ĪŖ3Mg£ØOH£©2+2Fe3+═3Mg2++2Fe£ØOH£©3£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ£ŗ ±¾Ģāæ¼²éĄė×Ó·“Ó¦ŹéŠ“µÄÕżĪóÅŠ¶Ļ£¬Ć÷Č··¢ÉśµÄ»Æѧ·“Ó¦ŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£¬×¢ŅāĪļÖŹµÄŠŌÖŹ¼°Ąė×Ó·“Ó¦µÄŹéŠ“·½·Ø£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠŅ»¹ĢĢå»ģŗĻĪļ£¬æÉÄÜÓÉNa2CO3”¢Na2SO4”¢CuSO4”¢CaCl2”¢NaCl»ģŗĻ¶ų³É£®ĪŖ¼ģŃéĖüĆĒµÄ×é³É£¬×öĮĖŅŌĻĀŹµŃé£ŗ
£Ø1£©½«¹ĢĢå»ģŗĻĪļČÜÓŚĖ®£¬½Į°čŗóµĆµ½ĪŽÉ«ĶøĆ÷ČÜŅŗ£»
£Ø2£©Ķł“ĖČÜŅŗÖŠµĪ¼ÓĻõĖį±µČÜŅŗ£¬ÓŠ°×É«³ĮµķÉś³É£»
£Ø3£©ĶłÉś³É³ĮµķµÄŹŌ¹ÜÖŠ¼Ó×ćĮæĻ”ĻõĖį£¬³ĮµķČ«²æČܽā£¬²¢ÓŠĪŽÉ«ĘųĢå²śÉś£®
ŹŌÅŠ¶Ļ£ŗ¹ĢĢå»ģŗĻĪļÖŠæĻ¶ØÓŠ£ØĢī·Ö×ÓŹ½£© £¬æĻ¶Øƻӊ £®
µŚ£Ø2£©²½ŹµŃé·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ
µŚ£Ø3£©²½ŹµŃé·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĪļÖŹµÄĮæÅضČĻąĶ¬µÄĻĀĮŠČÜŅŗ¢Ł£ØNH4£©2CO3 ¢Ś£ØNH4£©2SO4¢ŪNH4HCO3 ¢ÜNH4HSO4¢ŻNH4Cl ¢ŽNH3•H2O£»°“c£ØNH4+£©ÓÉŠ”µ½“óµÄÅÅĮŠĖ³ŠņÕżČ·µÄŹĒ£Ø£©
A£® ¢Ū¢Ż¢Ü¢Ž¢Ł¢Ū B£® ¢Ž¢Ż¢Ū¢Ü¢Ł¢Ś C£® ¢Ž¢Ū¢Ż¢Ü¢Ł¢Ś D£® ¢Ž¢Ū¢Ż¢Ü¢Ś¢Ł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ČēĶ¼1ĖłŹ¾£¬Ä³Ķ¬Ń§Éč¼ĘĮĖŅ»øöČ¼ĮĻµē³Ų²¢Ģ½¾æĀČ¼ī¹¤ŅµŌĄķŗĶ“ÖĶµÄ¾«Į¶ŌĄķ£¬ĘäÖŠŅŅ×°ÖĆÖŠXĪŖŃōĄė×Ó½»»»Ä¤£®Ēė°“ŅŖĒó»Ų“šĻą¹ŲĪŹĢā£ŗ
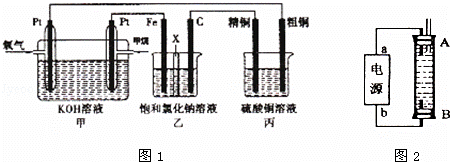
£Ø1£©¼×ĶéČ¼ĮĻµē³Ųøŗ¼«µē¼«·“Ó¦Ź½ŹĒ£ŗ £»
£Ø2£©ŹÆÄ«µē¼«£ØC£©µÄµē¼«·“Ó¦Ź½ĪŖ £»
£Ø3£©ČōŌŚ±ź×¼×“æöĻĀ£¬ÓŠ2.24LŃõĘų²Ī¼Ó·“Ó¦£¬ŌņŅŅ×°ÖĆÖŠĢśµē¼«ÉĻÉś³ÉµÄĘųĢåĢå»żĪŖ L£»±ū×°ÖĆÖŠŅõ¼«Īö³öĶµÄÖŹĮæĪŖ g£»
£Ø4£©Ä³Ķ¬Ń§Ąū¼×ĶéČ¼ĮĻµē³ŲÉč¼Ęµē½ā·ØÖĘČ”ĘÆ°×Ņŗ»ņFe£ØOH£©2µÄŹµŃé×°ÖĆ£ØČēĶ¼2ĖłŹ¾£©£®
ČōÓĆÓŚÖĘĘÆ°×ŅŗŹ±aĪŖµē³Ųøŗ¼«£¬µē½āÖŹČÜŅŗ×īŗĆÓĆ £®
ČōÓĆÓŚÖĘFe£ØOH£©2£¬Ź¹ÓĆĮņĖįÄĘ×öµē½āÖŹČÜŅŗ£¬Ńō¼«Ń”ÓĆĢś×÷µē¼«£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ£¬ŌŚČÜŅŗÖŠæÉ·¢ÉśŅŌĻĀ·“Ó¦£ŗ¢ŁH++Z﹣+XO4﹣=X2++Z2+H2O£ØĪ“ÅäĘ½£©£¬¢Ś2M2++R2=2M3++2R﹣£¬¢Ū2R﹣+Z2=R2+2Z﹣£¬ÓÉ“ĖÅŠ¶ĻĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©
A£® ³£ĪĀĻĀ·“Ó¦2M2++Z2=2M3++2Z﹣²»æÉŅŌ×Ō·¢½ųŠŠ
B£® RŌŖĖŲŌŚ·“Ó¦¢ŚÖŠ±»Ńõ»Æ£¬ŌŚ¢ŪÖŠ±»»¹Ō
C£® ·“Ó¦¢ŁÅäĘ½ŗó£¬H2OµÄ»Æѧ¼ĘĮæŹżĪŖ8
D£® »¹ŌŠŌĒæČõĖ³ŠņĪŖ£ŗX2+£¾Z﹣£¾R﹣£¾M2+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆFeCl3ČÜŅŗøÆŹ“Ó”Ė¢µēĀ·°åÉĻµÄĶ£¬ĖłµĆµÄČÜŅŗÖŠ¼ÓČėĢś·Ū£®¶Ō¼ÓČėĢś·Ū³ä·Ö·“Ó¦ŗóµÄČÜŅŗ·ÖĪöŗĻĄķµÄŹĒ£Ø£©
A£® ČōĪŽ¹ĢĢåŹ£Óą£¬ŌņČÜŅŗÖŠŅ»¶ØÓŠFe3+
B£® ČōÓŠ¹ĢĢå“ęŌŚ£¬ŌņČÜŅŗÖŠŅ»¶ØÓŠFe2+
C£® ČōČÜŅŗÖŠÓŠCu2+£¬ŌņŅ»¶Øƻӊ¹ĢĢåĪö³ö
D£® ČōČÜŅŗÖŠÓŠFe2+£¬ŌņŅ»¶ØÓŠCuĪö³ö
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
I£®ĻĀĮŠĪļÖŹÖŠŹōÓŚĒæµē½āÖŹµÄŹĒ £»ŹōÓŚČõµē½āÖŹµÄŹĒ £»ŹōÓŚ·Ēµē½āÖŹµÄŹĒ £®£ØĢīŠņŗÅ£© ¢Ł°±Ęų ¢Ś°±Ė® ¢ŪŃĪĖį ¢Ü“×Ėį ¢ŻĮņĖį±µ ¢ŽŅų ¢ßĀČ»ÆÄĘ ¢ą¶žŃõ»ÆĢ¼ ¢į“×Ėįļ§ ¢āĒāĘų
II£®Ä³·“Ó¦ĢåĻµÖŠµÄĪļÖŹÓŠ£ŗCr2£ØSO4£©3”¢K2S2O8”¢K2Cr2O7”¢K2SO4”¢H2SO4”¢H2O£®ŅŃÖŖK2S2O8µÄŃõ»ÆŠŌ±ČK2Cr2O7Ē森
£Ø1£©Ēė½«ŅŌÉĻ·“Ó¦ĪļÓėÉś³ÉĪļ±ąŠ“³ÉŅ»øöŃõ»Æ»¹Ō·“Ó¦·½³ĢŹ½£Ø²»ŅŖĒóÅäĘ½£©
£Ø2£©·“Ó¦ÖŠ£¬±»»¹ŌµÄĪļÖŹŹĒ ŹĒ
£Ø3£©ŌŚĖįŠŌĢõ¼žĻĀK2Cr2O7Óė²ŻĖį£ØH2C2O4£©·“Ó¦µÄ²śĪļŹĒ£ŗCr2£ØSO4£©3”¢CO2”¢K2SO4ŗĶH2O£¬Ōņ»¹Ō¼ĮÓėŃõ»Æ¼ĮĪļÖŹµÄĮæÖ®±ČĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Li”«SO2µē³Ų¾ßÓŠŹä³ö¹¦ĀŹøßĒŅµĶĪĀŠŌÄÜŗĆĢŲµć£¬Ęäµē½āÖŹĪŖLiBr£¬ČܼĮŹĒĢ¼Ėį±ūĻ©õ„ŗĶŅŅėę£¬Li+æÉŌŚĘäÖŠŅĘ¶Æ£®µē³Ų×Ü·“Ó¦Ź½ĪŖ£ŗ2Li+2SO2 Li2S2O4ĻĀĮŠÓŠ¹Ųµē³ŲµÄĖµ·ØÕżČ·µÄŹĒ£Ø£©
Li2S2O4ĻĀĮŠÓŠ¹Ųµē³ŲµÄĖµ·ØÕżČ·µÄŹĒ£Ø£©
A£® øƵē³Ų×Ü·“Ó¦ĪŖæÉÄę·“Ó¦
B£® ³äµēŹ±Ņõ¼«·“Ó¦Ź½ĪŖ£ŗLi++e﹣═Li
C£® ·ÅµēŹ±Li+Ļņøŗ¼«ŅʶÆ
D£® øƵē³Ųµē½āÖŹČÜŅŗæÉ»»³ÉLiBrĖ®ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
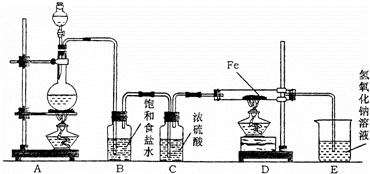
Ä³ŃŠ¾æŠŌѧĻ°Š”×éÉč¼ĘČēĶ¼×°ÖĆÖĘČ”ĀČĘų²¢ŅŌĀČĘųĪŖŌĮĻ½ųŠŠŹµŃ飮
£Ø1£©×°ÖĆAÉÕĘæÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £»
£Ø2£©×°ÖĆBÖŠ±„ŗĶŹ³ŃĪĖ®µÄ×÷ÓĆŹĒ £¬×°ÖĆCÖŠÅØĮņĖįµÄ×÷ÓĆŹĒ £»
£Ø3£©ŹµŃ鏱£¬ĻȵćČ¼A“¦µÄ¾Ę¾«µĘ£¬ŌŁµćČ¼D“¦¾Ę¾«µĘ£¬Š“³öDÖŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½ £¬Š“³öEÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ £»
£Ø4£©ČōŹµŃéÖŠÓĆ12mol•L﹣1ÅØŃĪĖį10mLÓė×ćĮæµÄMnO2·“Ó¦£¬Éś³ÉCl2µÄĪļÖŹµÄĮæ×ÜŹĒŠ”ÓŚ0.03mol£¬ŹŌ·ÖĪöæÉÄÜ“ęŌŚµÄŌŅņŹĒ£ŗ¢Ł £¬¢Ś £®
ÓūŹ¹·“Ӧɜ³ÉCl2µÄĪļÖŹµÄĮæ×ī“ó³Ģ¶ČµÄ½Ó½ü0.03mol£¬ŌņŌŚ×°ÖĆĘųĆÜŠŌĮ¼ŗƵÄĒ°ĢįĻĀŹµŃéÖŠÓ¦²ÉČ”µÄ“ėŹ©ŹĒ £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com